Кристаллизационные методы разделения смесей
a0=[xк(1-xм)]/[xм(1-xк)]. (1) На практике, однако, равновесие обычно не достигается, т.к. на степень разделения оказывают влияние скорость кристаллизации, интенсивность перемешивания р-ра или расплава, величина захвата маточной жидкости кристаллами, концентрация смеси и др.
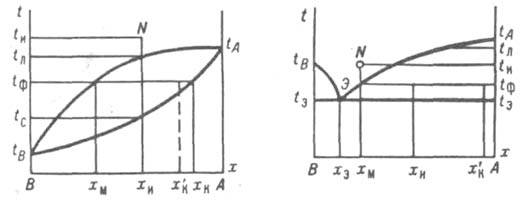
Рис. 1. Диаграмма т-ра состав для бинарных смесей, образующих твердые
р-ры.
Рис. 2. Диаграмма т-ра - состав для эвтектич. смесей.
Поэтому концентрация осн. компонента в образующихся кристаллах х'к всегда (при a0>1) меньше равновесного значения хк, и реальный, или эффективный, коэф. разделения составляет:
aэ=[x'к(1-xм)]/[xм(1-x'к)]. (2) Если содержание осн. компонента значительно превышает концентрации остальных компонентов (в таких случаях они являются примесями), процесс разделения наз. очисткой, и ур-ние (1) упрощается:
Фракционная кристаллизация.
Различают след. виды фракционной кристаллизации: массовую, на охлаждаемых пов-стях, направленную, зонную плавку.
Массовая кристаллизация. Метод состоит в одновременном получении большого кол-ва кристаллов во всем объеме аппарата. В пром-сти реализовано неск. вариантов массовой кристаллизации, к-рую осуществляют в периодически или непрерывно действующих аппаратах: емкостных, снабженных наружными охлаждающими рубашками либо внутр. змеевиками и часто перемешивающими устройствами; трубчатых, скребковых, дисковых, шнековых и др. Из-за отсутствия методики расчета параметр aэ при массовой кристаллизации находят экспериментально.
Кристаллизация с теплопередачей через стенку. В случае расплавов процесс проводят их охлаждением. При кристаллизации р-ров выбор режима процесса определяется гл. обр. характером зависимости р-римости в-в от т-ры. Если р-римость в-ва мало изменяется с изменением т-ры (напр., NaCl в воде), кристаллизацию осуществляют частичным или практически полным выпариванием насыщ. р-ра при постоянной т-ре (изотермич. кристаллизация). В-ва, р-римость к-рых сильно зависит от т-ры (напр., KNO3 в воде), кристаллизуют охлаждением горячих р-ров, при этом исходное кол-во р-рителя, к-рый содержится в маточной жидкости, в системе не изменяется (изогидрич. кристаллизация). Образовавшиеся кристаллы в зависимости от их св-в, формы и условий проведения процесса захватывают разл. кол-во маточного р-ра. Содержание его в твердой фазе в виде включений в порах, трещинах и полостях существенно зависит от способа разделения кристаллов и маточной жидкости. Так, при отделении кристаллов на барабанном вакуум-фильтре концентрация в них маточного р-ра составляет 10-30%, на фильтрующей центрифуге - 3-10%.
Осн. достоинства процесса: высокая производительность, отсутствие контакта разделяемой смеси и хладагента, простота аппаратурного оформления; недостатки: сравнительно невысокие коэф. теплопередачи, инкрустация пов-стей охлаждения, большой захват маточной жидкости кристаллами, необходимость установки дополнит. оборудования для разделения твердой и жидкой фаз, недостаточно высокий выход кристаллич. продукта. Примеры применения: получение хлоридов К и Na из сильвинита, разделение изомеров ксилола.
Контактная кристаллизация. Процесс осуществляют при непосредственном контакте р-ра или расплава с разл. хладагентами. В качестве последних используют охлажденные жидкости (обычно вода либо водные р-ры минер, солей), не смешивающиеся и не взаимод. с разделяемой смесью, а также сжиженные газы (напр., бутан), к-рые при смешении с ней испаряются. Осн. достоинства процесса: интенсификация теплообмена, более высокая скорость в отличие от кристаллизации с теплопередачей через стенку, высокий выход кристаллич. продукта, простота аппаратурного оформления; недостатки: необходимость отделения хладагента от маточного р-ра, возможность загрязнения целевого продукта. Примеры применения:
очистка сырого бензола, разделение смесей нафталина с бензолом, толуолом или b-метилнафталином, опреснение морской воды.
Кристаллизация на охлаждаемых поверхностях. Особенность метода заключается в том, что т-ра разделяемой смеси постоянно немного превышает т-ру начала кристаллизации. Поэтому зарождение и рост кристаллов происходят не во всем объеме аппарата, как при массовой кристаллизации, а только на его охлаждаемых пов-стях. Различают кристаллизацию на неподвижных и подвижных пов-стях и пленочную.
Кристаллизация на неподвижных пов-стях. Процесс проводят в аппаратах периодич. действия, где охлаждающими элементами обычно служат гладкие или ребристые трубы либо змеевики. Исходную смесь подают в аппарат и весьма долго выдерживают в нем, пока на охлаждаемых пов-стях не образуется довольно большой слой кристаллов. Затем маточную жидкость сливают, а кристаллы выводят из аппарата. Осн. достоинства: отсутствие стадии отделения кристаллич. фазы от маточного р-ра (это преимущество отличает и др. варианты данного процесса от массовой кристаллизации), простота аппаратурного оформления; недостатки: большая продолжительность процесса, значит. захват маточной жидкости кристаллами. Примеры применения: разделение изомеров нитрохлорбен-зола, нафталина и бензойной к-ты.
Кристаллизация на подвижных пов-стях. Процесс осуществляют в аппаратах, снабженных охлаждаемыми вращающимися барабанами. Горячая исходная смесь поступает в ванну кристаллизатора, в к-рую погружен барабан. Образующийся на его пов-сти кристаллич. слой срезается спец. ножом. Осн. достоинства процесса: высокие интенсивность теплообмена и производительность, возможность реализации непрерывного варианта; недостаток - невозможность в ряде случаев достижения высокой степени фракционирования (т.к. вся маточная жидкость, захватываемая барабаном, переходит в кристаллич. фазу). Эффективность разделения можно повысить внеш. обогревом и отжимом посредством спец. валиков поднимающегося на барабане слоя кристаллов. Примеры применения: разделение смесей b-метилнафталина с a-метилнафталином, нафталина с дифенилом.
Пленочная кристаллизация. Процесс проводят в вертикальном кожухотрубчатом теплообменнике, снабженном спец. оросит, устройством. С его помощью исходная смесь равномерно распределяется по внутр. пов-сти всех труб и стекает по их стенкам в виде тонкой пленки. В межтрубное пространство кристаллизатора подается охлаждающая жидкость. При охлаждении начинается частичная кристаллизация смеси, и внутр. пов-сть труб покрывается ровным слоем кристаллов. По достижении заданной толщины слоя подача разделяемой смеси прекращается, в межтрубное пространство поступает греющий агент (напр., вода или водяной пар), происходит выплавление кристаллич. фазы. В случае бинарных смесей в оптим. условиях (при плоском фронте кристаллизации) параметр aэ можно рассчитать по ур-нию (при xи<<1):
aэ=a0/[a0+(1-a0)ехр(- vdD/D)], (З) где v - линейная скорость кристаллизации, dD - толщина диффузионного пограничного слоя, D - коэф. диффузии примеси в жидкой фазе.
Осн. достоинства процесса: возможность достижения aэ, близких к a0, высокая производительность, возможность полной автоматизации; недостатки: чувствительность к равномерности орошения по всем трубам, значит. металлоемкость и относит. сложность технол. оборудования. Примеры применения: разделение и очистка в-в в произ-вах капролактама, фенола, нитро- и хлорароматич. соединений, концентрирование водных р-ров вымораживанием и др.
Направленная кристаллизация. Процесс обычно осуществляют в горизонтальных или вертикальных (рис. 3) контейнерах, выполненных из термостойкого стекла, кварца, керамики, фторопласта либо графита. Контейнеры, в к-рые
загружены образцы очищаемого в-ва, медленно движутся из зоны нагревания в зону охлаждения, на границе к-рых происходит кристаллизация. Фронт кристаллизации при интенсивном перемешивании жидкой фазы постепенно перемещается от одного конца расплавленного образца к другому вследствие принудительного (обычно с помощью мех. привода) движения контейнера. При этом примеси, содержащиеся в в-ве, перераспределяются по длине кристаллизующегося образца. Если фронт кристаллизации близок к плоскому, значение aэ можно рассчитать по ур-нию (2). Если параметр aэ не зависит от концентрации примеси и в ходе процесса остается постоянным, изменение состава по длине образца определяется выражением:
xв=xиaэ(1-g)aэ-1, (4) где g-доля закристаллизовавшегося образца.
По окончании кристаллизации часть образца, обогащенную примесями, отделяют, а остальное кол-во переплавляют. С целью увеличения степени очистки процесс иногда многократно повторяют. Осн. достоинства: обеспечение глубокой очистки в-в, возможность очистки как высокоплавких, так и низкоплавких соединений; недостатки: значит. потери в-ва в случае повторения кристаллизации из-за необходимости каждый раз отделять загрязненную часть образца, большая продолжительность процесса, низкая производительность, высокая стоимость разделения. К направленной кристаллизации прибегают, как правило, для получения небольших кол-в в-в высокой чистоты в случае невозможности использования др. К.м. (в частности, зонной плавки), напр. при очистке металлов (Tl, Sb) и орг. соединений, а также для выращивания монокристаллов (GaAs, InP, LiF, стильбен).
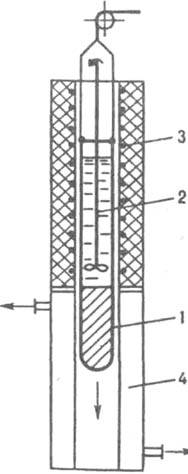
Рис. 3. Установка для направленной кристаллизации: 1 - контейнер; 2 - мешалка; 3, 4 - секции соотв. нагревания и охлаждения.
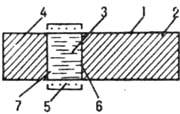
Зонная плавка (зонная перекристаллизация). Процесс проводят путем медленного перемещения вдоль твердого удлиненного образца (слитка) узкой расплавленной зоны, создаваемой спец. нагревателями (рис. 4). При этом в отличие от направленной кристаллизации образуются две подвижные межфазные границы: на одной происходит плавление, на другой - кристаллизация. В результате после одного прохода расплавленной зоны примесь в образце
Рис. 4. Схема зонной плавки: 1 - контейнер; 2 - исходный образец; 3 - расплавленная зона; 4 - кристаллич. фаза после очистки; 5 - нагреватель; 6 - 7 - соотв. границы плавления и кристаллизации.
перераспределяется, причем наблюдаются три участка. При aэ<1 концентрация примеси на первом, среднем и третьем участках соотв. снижается, постоянна и повышается (на длине образца, равной ширине расплавленной зоны); при aэ>1 наиб. концентрация примеси создается в начале образца, наименьшая - в конце его.
Для достижения высокой степени очистки обычно производят неск. проходов расплавленной зоны. При очень большом числе проходов п обеспечивается предельное распределение примеси по длине образца, выражаемое экспоненциальным законом:
xn=:(z)=Aexp(Bz), (5) где хn=: - концентрация примеси в сечении с координатой z по длине образца, А и B - постоянные, зависящие от xи, aэ, длины образца и ширины расплавленной зоны. В отличие от направленной кристаллизации повторные проходы расплавленной зоны можно осуществлять без удаления загрязненной части образца, т. к. каждый раз расплавляется лишь его узкая зона. По достижении необходимого распределения концентрации примеси вдоль образца последний извлекают из контейнера, сильно загрязненную часть его удаляют, а остальное кол-во расплавляют для гомогенизации состава. Осн. достоинство - высокая эффективность; недостатки: низкая производительность, большая продолжительность, высокая стоимость. Примеры применения: получение особо чистых в-в с содержанием примесей 10-7 — 10-9 % (металлы - Gе, Bi, Те, полупроводники - GaP, InAs), лаб. очистка разл. соед. (бензойная к-та, нафталин), выращивание монокристаллов (Si, BeO, сапфир, корунд), концентрирование микропримесей в хим. анализе, исследование диаграмм состояния. наиб. целесообразно зонную плавку использовать для глубокой очистки в-в, предварительно очищенных др. К.м. до концентраций примесей приблизительно 1%.
Кристаллизация в присутствии вспомогательных веществ. Разделение смесей методами фракционной кристаллизации иногда невозможно или затруднено. В таких случаях фракционирование проводят, добавляя в р-р или расплав спец. вспомогат. в-ва. Различают аддуктивную и экстрактивную кристаллизацию.
Аддуктивная кристаллизация. Метод основан на способности одного или неск. компонентов разделяемой смеси образовывать с к.-л. дополнительно вводимым в-вом мол. комплексы либо клатраты (канальные, клеточные). Получаемая при этом кристаллич. фаза распадается при нагр. на индивидуальные компоненты.
Склонность ряда в-в к образованию мол. соед. при кристаллизации используют в осн. для фракционирования нек-рых смесей орг. в-в. Так, для выделения n-ксилола из его смеси с изомерами в расплав вводят ССl4 или SbBr3, образующие с n-ксилолом мол. соед., но не взаимодействующие с м- и o-ксилолами. В качестве клатратообразующих в-в применяют карбамид, гидрохинон, металлоорг. соед. и др. Напр., способность карбамида образовывать комплексы с углеводородами и их производными широко используют для выделения парафинов из нефтепродуктов (см. Депарафнизация). Смеси неорг. соед. часто разделяют с помощью гидрохинона, к-рый дает устойчивые клатраты, напр., с SO2, О2, HCl, H2S, а также с благородными газами (Аr, Кr, Хе). Для фракционирования смесей ароматич. соед., в частности для извлечения бензола, применяют комплекс Ni(CN)2.NH3.C6H6. Нек-рые газы (пропан, хладоны) и низкокипящис жидкости образуют кристаллич. комплексы с водой (см. Газовые гидраты) при т-рах, значительно превышающих т-ру ее замерзания. Это используют, напр., для опреснения морской воды.
Аддуктивная кристаллизация обычно проводится в емкостных аппаратах для массовой кристаллизации и включает след. стадии: смешение разделяемой смеси со вспомогат. в-вом, образование кристаллич. осадка, отделение его от маточника, промывку осадка и его разложение, отделение продукта от вспомогат. в-ва. Недостатки: высокие уд. расход (10-20 кг на 1 кг кристаллич. продукта) и стоимость вспомогат. в-в. большое число стадий.
Экстрактивная кристаллизация. Сущность метода заключается в изменении фазового равновесия в разделяемой системе при введении в нее вспомогат. в-в. Процесс осуществляют в обычной кристаллизац. аппаратуре в двух вариантах: по одному из них дополнит. компонентом служит р-ритель, образующий с исходной смесью гомог. р-р, по другому - экстрагент, растворяющий примеси, но не смешивающийся с осн. компонентом. В первом случае принципиальная
технол. схема включает след. стадии: разделение, напр., бинарной смеси массовой кристаллизацией на один чистый компонент и первый маточник, смешение последнего с вспомогат. в-вом, кристаллизацию тройной смеси с выделением др. чистого компонента, регенерацию р-рителя из второго маточника, смешение остатка, содержащего нек-рые кол-ва обоих компонентов, с исходной смесью. Во втором случае в результате смешения разделяемой системы с экстрагентом образуется гетерог. смесь и возникают два слоя: один содержит очищенный продукт, другой - преим. нежелательные примеси и экстрагент. При этом разделение исходной смеси осуществляется за счет суммарного эффекта экстракции и кристаллизации. Процесс имеет такие же недостатки, как и аддуктивная кристаллизация.
Экстрактивную кристаллизацию применяют для фракционирования смесей, образующих эвтектики (напр., смесь м- я n-ксилолов, р-ритель - н-гептан) и мол. комплексы (напр., смесь м- и n-крезолов, р-ритель - уксусная к-та). Довольно часто экстрактивную кристаллизацию сочетают с массовой и направленной кристаллизацией, а также с зонной плавкой, что значительно повышает эффективность очистки в-в с помощью указанных методов. Так, экстрактивную зонную перекристаллизацию с р-рителями (бензол, нафталин) используют для очистки насыщ. углеводородов и полистирола, экстрактивные направленную кристаллизацию а зонную плавку с экстрагентами - для очистки металлов (вспомогат. в-ва - легкоплавкие металлы, соли, оксиды) и разнообразных орг. в-в (экстрагенты - те же, что и при экстракции жидкостной, напр. трибутилфосфат, нафтеновые к-ты, алкилфенолы, первичные и вторичные амины).
Фракционные плавление и сублимация. Фракционное плавление. Деление методов разделения смесей на фракционные кристаллизацию и плавление условно, т.к. эти методы обычно взаимосвязаны. Рассматриваемый процесс проводят путем частичного медленного выплавления предварительно закристаллизованного расплава в аппаратах с внутр. теплообменными устройствами, камерах "потения", трубчатых (в т.ч. пленочных) и др. При этом разделение может происходить в одном или неск. аппаратах. В первом случае исходная смесь сначала охлаждается до полного или частичного затвердевания. Далее образовавшаяся кристаллич. фаза медленно нагревается, причем часть ее (преим. низкоплавкий компонент) переходит в жидкое состояние, отделяется от кристаллов и свободно стекает Оставшаяся часть твердой фазы (обогащенная высокоплавким компонентом) при быстром нагреве полностью расплавляется и отводится из аппарата в виде конечного продукта. Во втором случае расплав предварительно полностью отверждается на барабанном или ленточном кристаллизаторе, затем кристаллич. масса медленно нагревается в спец. аппарате, частично расплавляясь. Полученную суспензию обычно выдерживают в течение определенного времени при т-ре выше tс и далее подвергают фильтрованию. После отделения жидкости остается кристаллич. продукт, обогащенный высокоплавким компонентом.
Осн. достоинство процесса - возможность сочетания преимуществ фракционной кристаллизации и плавления, высокая производительность; недостаток - невозможность эффективного разделения смесей, образующих твердые р-ры. Примеры применения: отделение парафина от нефтяных масел, очистка сырого бензола от примесей (в частности, серосодержащих), очистка восков, выделение нафталина из его фракций и др.
Фракционная сублимация. Метод состоит в частичном испарении твердой исходной смеси. Сублимация неразрывно связана с кристаллизацией из газовой фазы - десублимацией, при к-рой зарождение и рост кристаллов происходят во всем объеме аппарата или только на его охлаждаемых пов-стях. Установка для сублимации (рис. 5) состоит из бункера, куда поступает разделяемая смесь, сублиматора и вспомогат. емкостей. Сублиматор - труба с вращающимся шнеком,
перемещающим смесь из левой секции аппарата, к-рая обогревается электрич. током, в правую, снабженную охлаждающим устройством. Т. обр., на пути от места загрузки примерно до середины сублиматора твердая смесь частично испаряется. В правой секции из газовой фазы конденсируется готовый продукт, к-рый срезается шнеком со стенок аппарата и направляется в спец. сборник; оставшаяся после сублимации масса выгружается в емкость для отвала.
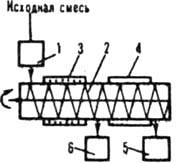
Рис. 5. Установка для сублимация: 1 - бункер; 2 - сублиматор с обогреваемой злекрич. током (3) и охлаждаемой (4) секциями; 5, 6 - сборники соотв. готового продукта в отвала.
Осн. достоинство - большая эффективность разделения (как правило, для систем твердое тело - газ она всегда выше, чем для систем твердое тело - жидкость); недостаток - значительно большие по сравнению с фракционными кристаллизацией и плавлением затраты энергии. Примеры применения: очцстка от примесей промежут. продуктов в произ-вах красителей (антрахинона, бензантрона, 2 - метилантрахинона и др.), очистка терефталевой и бензойной к-т (фракционная десублимация). По аналогии с противоточной кристаллизацией (см. ниже) перспективно использование противоточной сублимации с непрерывным массообменом между кристаллами и паровой фазой (напр., разделение систем Zr—Hf, антрацен - карбазол, очистка АlСl3).
Многократная перекристаллизация Методы однократных кристаллизации и плавления часто не. обеспечивают требуемой степени разделения смесей или достаточного выхода целевого компонента. Для улучшения этих показателей применяют многократную перекристаллизацию р-ров или расплавов, что дает возможность получать целевые продукты с содержанием осн. в-ва 99% и более.
Один из вариантов многократной перекристаллизации -дробная кристаллизация, осуществляемая только из р-ров. По этому методу исходную смесь разделяют путем массовой кристаллизации на две фракции - кристаллич. фазу и маточную жидкость; каждую из них делят на две новые фракции (соотв. добавлением к кристаллам свежего р-рителя с повторной кристаллизацией и выпариванием маточника). Такое дробление продолжают до тех пор, пока не достигают необходимой степени разделения. Условие построения рациональной технол. схемы - требование минимума числа фракций при заданном числе ступеней (кристаллизаторов). Для этого процесс проводят таким образом, чтобы отдельные промежут. фракции имели одинаковые составы и могли быть объединены. Осн. достоинство процесса - возможность разделения смесей неск. компонентов с близкими физ.-хим. св-вами (напр., смесей Zr и Hf или РЗЭ); недостатки: низкая производительность, большое число стадий.
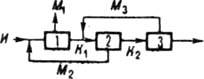
Рис. 6. Схема многократной перекристаллизации.
Для повышения производительности используют многократную перекристаллизацию с рециркуляцией кристаллов (маточника), осуществляемой в неск. последовательно соединенных аппаратах - ступенях (рис. 6). Исходная эвтектич. смесь И подается в ступень l, где образуются кристаллы K1 последние после отделения от маточника M1 расплавляются и поступают на кристаллизацию в ступень 2,
а выделившиеся в ней кристаллы K2 - в ступень 3. Маточники M2 и М3 направляются на вход в предыдущие ступени, а продукт П выводится из ступени 3. Для разделения смесей, образующих твердые р-ры, на индивидуальные компоненты применяют многократную перекристаллизацию с противотоком маточной жидкости и твердой фазы и возвратом части готового продукта. Осн. достоинство многократной перекристаллизации - возможность достижения высоких степеней очистки; недостаток - большая продолжительность. Противоточная кристаллизация с непрерывным массообменом. Многократная перекристаллизация с противоточным движением кристаллич. фазы и маточного р-ра м.б. осуществлена в одном аппарате с непрерывным межфазным массообменом. По принципу действия противоточные кристаллизаторы аналогичны насадочным ректификац. колоннам (см. Носадочные аппараты). Кристаллы, образующиеся при охлаждении в верх, части шнекового кристаллизатора (рис. 7), перемещаются в ниж. часть аппарата, где они плавятся, и расплав поднимается вверх навстречу кристаллам. Исходная смесь с концентрацией хп подается в среднюю часть кристаллизатора, высокоплавкий продукт с концентрацией хп выводится снизу, а низко плавкий с концентрацией хи - сверху. В лаб. шнековых аппаратах и пустотелых колоннах с транспортом кристаллов под действием силы тяжести, диаметр к-рых не превышает 30 см, высокие степени разделения достигаются даже в случае смесей, образующих твердые р-ры (системы бензол - тиофен и n-дихлорбензол-n-дибромбензол удалось разделить на практически чистые компоненты). С увеличением диаметра колонн эффективность фракционирования снижается вследствие продольного перемешивания, каналообразования и слипания кристаллов.
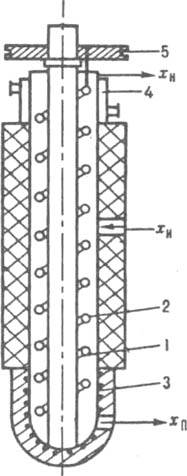
Рис. 7. Колонный шнековый кристаллизатор: 1 - корпус; 2 - шнек; 3, 4 - секции соотв. нагревания и охлаждения; 5 - привод.
В пром. практике для очистки смесей (напр., изомеров дихлорбензола) наиб. распространены комбинир. установки, к-рые состоят из двух-трех охлаждаемых горизонтальных шнековых кристаллизаторов диаметром до 2 м и вертикаль ной очистной колонны с гравитац. перемещением кристаллов. На таких установках расход энергии не превышает 5-10% от энергетич. затрат на ректификац. установках. Макс. пропускной способностью обладают пульсационные аппараты колонного типа, в к-рых с помощью спец. устройства интенсифицируется межфазный массообмeн. Осн. достоинства противоточной кристаллизации по сравнению с др. методами: наиб. эффективность разделения, высокая производительность; недостаток-сложность аппаратурного оформления. Лит.: Пфанн В., Зонная плавка, 2 изд.. пер. с англ.. М.. 1970; Вигдорович В. Н., Совершенствование зонной перекристаллизации, М., 1974; Гельперин Н. И., Носов Г. А., Основы техники кристаллизации расплавов. М.. 1975; Девятых Г. Г., Еллиев Ю. Е., Введение в теорию глубокой очистки веществ, М., 1981; Гельперин Н. И., Ocнoвные процессы и аппараты химической технологии, кн. 2, М., 1981, с. 678-726; Пап Л., Концептрировиние вымораживанием, пер. с вент.. М., 1982; Тодес О. М.. Себалло В. А., Гольцикер А.Д., Массовая кристаллизация из растворов. Л., 1984; Гельперин Н. И., Носов Г. А., Основы техники фракционной кристаллизации, Мм 1986. В. А. Малюсов. С. К. Мясников.

