Кипение
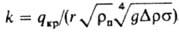 , где Dr
разность плотностей жидкости и пара. В первом приближении при К. в большом объеме насыщ. однородной маловязкой жидкости k=const (для воды, спирта и ряда др. сред k~0,14—0,16). В жидкости, осн. масса к-рой недогрета до т-ры К. на величину v=Ткип-Тж, параметр qкp~qкр,10(l+0,1 arп-0,75 К-1),
, где Dr
разность плотностей жидкости и пара. В первом приближении при К. в большом объеме насыщ. однородной маловязкой жидкости k=const (для воды, спирта и ряда др. сред k~0,14—0,16). В жидкости, осн. масса к-рой недогрета до т-ры К. на величину v=Ткип-Тж, параметр qкp~qкр,10(l+0,1 arп-0,75 К-1),
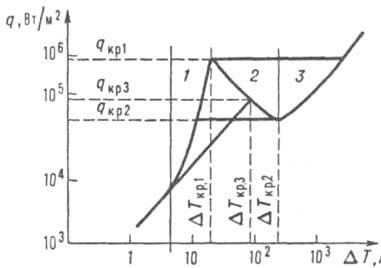
Рис. 1. Зависимость плотности теплового потока от разности т-р
DТ=Ти—Ткип при кипении в большом объеме свободно конвектирующей жидкости: 1 - пузырьковый режим; 2 - переходный режим, характеризуемый сменой пузырьковой структуры на пов-сти нагрева сплошным паровым слоем (пленкой), от к-рого отрываются крупные паровые пузыри; 3 - пленочный режим, при к-ром происходит также радиационная теплоотдача от пов-сти нагрева к жидкости через паровой слой; прямая линия характеризует третий кризис кипения.
где qкр,10 - плотность теплового потока при v=0, rп - отношение плотностей пара и жидкости, К=r/Cpv - тепловой критерий фазового перехода, Ср - массовая теплоемкость жидкости, ДжДкг.К).
При низких давлениях возможен третий кризис К. в форме непосредственного перехода от режима конвективного движения жидкости к развитому пленочному К. Этот переход имеет цепной кавитационный механизм и реализуется при разностях т-р на пов-сти нагрева и К., удовлетворяющих условию: 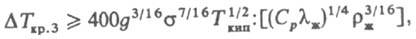 где lж и rж - соотв. теплопроводность и плотность перегретой жидкости, g - ускорение своб. падения.
Четвертый кризис К. связан с возникновением термодинамич. неустойчивости жидкой фазы при достижении нек-рой критич. пов-сти нагрева.
Критич. плотности тепловых потоков при К. в каналах существенно зависят от их форм и размеров, скорости течения жидкости и паросодержания потока. Универсальные закономерности здесь пока не установлены.
При своб. растекании жидкости по горячей пов-сти возникает т. наз. сфероидальное состояние - жидкость зависает над пов-стью нагрева под влиянием динамич. сопротивления образующегося пара (рис. 2). Время полного испарения данного начального объема жидкости определяется т-рой нагревателя.
где lж и rж - соотв. теплопроводность и плотность перегретой жидкости, g - ускорение своб. падения.
Четвертый кризис К. связан с возникновением термодинамич. неустойчивости жидкой фазы при достижении нек-рой критич. пов-сти нагрева.
Критич. плотности тепловых потоков при К. в каналах существенно зависят от их форм и размеров, скорости течения жидкости и паросодержания потока. Универсальные закономерности здесь пока не установлены.
При своб. растекании жидкости по горячей пов-сти возникает т. наз. сфероидальное состояние - жидкость зависает над пов-стью нагрева под влиянием динамич. сопротивления образующегося пара (рис. 2). Время полного испарения данного начального объема жидкости определяется т-рой нагревателя.
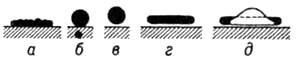
Рис. 2. Формы испарения жидкости, свободно растекающейся по горячей пов-сти: а в капле, смачивающей не сильно нагретую пов-сть, происходит пузырьковое кипение; б т-ра стенки повысилась, и капля принимает сферич форму; в при увеличении т-ры пов-сти нагрева капля зависает в паровом слое; г - с возрастанием объема капля принимает форму плоского сфероида; д взвешенный в паровом слое большой сфероид, из к-poro пар эвакуируется через куполообразные пузыри.
В технол. процессах используются оба вида поверхностного К. Напр., пленочное К. реализуется при жидкостной закалке металлич. изделий. Проектирование теплообменных аппаратов с принудит, заданием теплового потока (с выделением джоулевой теплоты, теплоты р-ции спонтанного распада ядерного топлива, в парогенераторах и т.п.) проводится в расчете на пузырьковый режим К. теплоносителя. Возникновение пленочного К., напр. при сбросе давления, может вызвать аварийную ситуацию.
Термогидродинамика К. р-ров и чистых жидкостей существенно различна. Так, для нек-рых р-ров и эмульсий критич. плотность теплового потока зависит от концентрации компонентов немонотонно, т.е. возможно существование экстремумов, причем максимум qкp, м. б. значительно больше, чем критич. значение теплового потока для каждого компонента в отдельности (рис. 3). При растворении в жидкости нелетучего в-ва снижается давление ее насыщ. пара и повышается Ткип. Это позволяет определять мол. м.
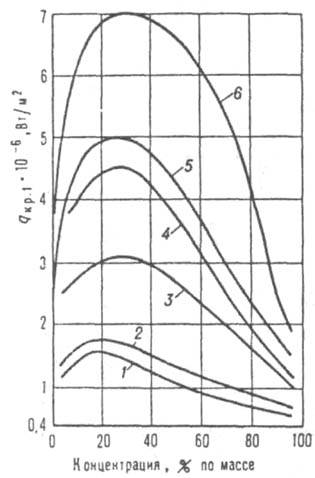
Рис. 3. Зависимость qкр,1, от массовой концентрации спирта в воде при своб. конвекции в большом объеме и разных пов-стях нагрева: /, 3. 5 вертикальная пластина соотв. при давлениях 98,1100 и 3100 кПа; 2, 4, б проволока диаметром 0,5 мм при таких же давлениях.
растворенных в-в по вызываемому ими повышению Ткнп чистого р-рителя (см. Эиулиоскопия). Выпадение твердой фазы из р-ра на пов-сть нагрева приводит к снижению общего коэф. теплопередачи. В таких процессах температурный режим теплообменных аппаратов необходимо рассчитывать в соответствии с диаграммой состояния данного раствора.
Режим К. существенно влияет на характер распространения акустич. волн в парожидкостной смеси. При этом волновые возмущения сопровождаются испарением и конденсацией на границах раздела фаз. Скорость звука в таких системах определяется соотношением между частотой волны и характерными временами процессов, обусловливающих фазовые переходы. Если частота настолько низка, что наложенное возмущение Dp вызывает изменение плотности Dr только за счет фазовых переходов, то скорость волны равна термодинамически равновесной скорости звука ае=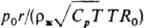 , где R0 уд. газовая постоянная, Дж/(кг.К). Если частоты волн таковы, что фазовые переходы практически не успевают происходить, то звук распространяется со скоростью
, где R0 уд. газовая постоянная, Дж/(кг.К). Если частоты волн таковы, что фазовые переходы практически не успевают происходить, то звук распространяется со скоростью 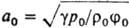 , где g - показатель адиабаты пара; j0 - объемное паросодержание смеси. Для реальных частот возмущений и состояний парожидкостной среды пузырьковой структуры скорость звука близка к значению aе, к-рое отличается от а0 примерно на два порядка. Так, для j0~0,1 величина ав=1 м/с при а0~100 м/с. Фазовые переходы влияют на динамику и структуру акустич. волн. Эти структуры обобщаются в виде спец. режимных карт
Лит. Скрипов В.П.. Метастабильная жидкость, М, 1972; Кутателадзе СС. Основы теории теплообмена, 5 изд., М., 1979; Кутателадзе СС НакоряковВЕ.. Тепломассообмен и волны в газожидкосгных системах, Новосиб.. 1984. C C Кутателадзе
, где g - показатель адиабаты пара; j0 - объемное паросодержание смеси. Для реальных частот возмущений и состояний парожидкостной среды пузырьковой структуры скорость звука близка к значению aе, к-рое отличается от а0 примерно на два порядка. Так, для j0~0,1 величина ав=1 м/с при а0~100 м/с. Фазовые переходы влияют на динамику и структуру акустич. волн. Эти структуры обобщаются в виде спец. режимных карт
Лит. Скрипов В.П.. Метастабильная жидкость, М, 1972; Кутателадзе СС. Основы теории теплообмена, 5 изд., М., 1979; Кутателадзе СС НакоряковВЕ.. Тепломассообмен и волны в газожидкосгных системах, Новосиб.. 1984. C C Кутателадзе

