Хлора оксиды
ХЛОРА ОКСИДЫ. Все X. о. имеют резкий
запах, термически и фотохимически нестабильны, склонны к взрывному распаду,
имеют положит.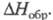 Монооксид [оксид С1(I), дихлороксид, гемиоксид] С12О - желто-оранжевый
газ со слабым зеленоватым оттенком, в жидком состоянии - красно-коричневый;
длина связи С1 — О 0,1700 нм, угол ОСlO 111°,
Монооксид [оксид С1(I), дихлороксид, гемиоксид] С12О - желто-оранжевый
газ со слабым зеленоватым оттенком, в жидком состоянии - красно-коричневый;
длина связи С1 — О 0,1700 нм, угол ОСlO 111°,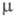 2,60
x 10-30 Кл x м (табл.); ур-ние температурной зависимости давления
пара lgp (мм рт. ст.) = 7,87 - 1373/Т (173-288 К); раств. в воде
с образованием НСЮ, р-римость (г в 100 г Н2О при 0 °С): 33,6
(2,66 кПа), 52,4 (6,65 кПа). При 60-100 °С термич. распад С12О
завершается за 12-24 ч, выше 110 °С через неск. мин происходит взрыв, освещение
ускоряет распад и повышает вероятность взрыва. С хлоридами образует оксихлориды,
напр., с Т1С14, ТаС15 и AsCl3 дает соотв.
Т1ОС12, ТаОС13 и AsO2Cl. С NO2
образует смесь NO2C1 и NO3C1, с N2O5
-чистый NO3C1. Фторированием С12О с помощью AgF2
можно получить C1OF3, а р-цией с AsF5 или SbF5
- соли хлорила ClO+2MF-6. Аналогично
реагируют с MF5 (где М - As и Sb) С1О2 и С12О6.
С насыщ. орг. соединениями С12О ведет себя как хлорирующий агент,
подобный хлору. Получают Сl2О пропусканием С12, разбавленного
N2, над HgO или р-цией С12 с влажным Na2CO3.
2,60
x 10-30 Кл x м (табл.); ур-ние температурной зависимости давления
пара lgp (мм рт. ст.) = 7,87 - 1373/Т (173-288 К); раств. в воде
с образованием НСЮ, р-римость (г в 100 г Н2О при 0 °С): 33,6
(2,66 кПа), 52,4 (6,65 кПа). При 60-100 °С термич. распад С12О
завершается за 12-24 ч, выше 110 °С через неск. мин происходит взрыв, освещение
ускоряет распад и повышает вероятность взрыва. С хлоридами образует оксихлориды,
напр., с Т1С14, ТаС15 и AsCl3 дает соотв.
Т1ОС12, ТаОС13 и AsO2Cl. С NO2
образует смесь NO2C1 и NO3C1, с N2O5
-чистый NO3C1. Фторированием С12О с помощью AgF2
можно получить C1OF3, а р-цией с AsF5 или SbF5
- соли хлорила ClO+2MF-6. Аналогично
реагируют с MF5 (где М - As и Sb) С1О2 и С12О6.
С насыщ. орг. соединениями С12О ведет себя как хлорирующий агент,
подобный хлору. Получают Сl2О пропусканием С12, разбавленного
N2, над HgO или р-цией С12 с влажным Na2CO3.
СВОЙСТВА ОКСИДОВ ХЛОРА
|
Показатель
|
Сl2О
|
СlO2
|
Сl2O4
|
Сl2O6
|
Сl2O7
|
|
|
Т. пл, оС
|
-120,6
|
-59
|
-117
|
3
|
-93,4
|
|
|
Т. кип., °С
|
2,0
|
9,7
|
44,5
|
203*
|
87
|
|
|
Плотн., г/см3
|
—
|
1,653 (5 °С)
|
1,82 (0°С)
|
2,023 (3,5 °С)
|
1,805** (25 °С)
|
|
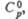 Дж/(моль х К)
Дж/(моль х К) |
47,81
|
42,00
|
86,03
|
|||
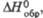 кДж/моль
кДж/моль |
81
|
93
|
180
|
310
|
240
|
|
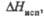 кДж/моль
кДж/моль |
26
|
26,3
|
30
|
40
|
34
|
|
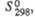 Дж/(моль х К)
Дж/(моль х К) |
267,84
|
256,77
|
327,23
|
—
|
—
|
*Расчетная. **2,38 г/см3 при -160 °С.
Диоксид С1О2 - желтый газ, в
жидком состоянии -ярко-красный, в твердом - красновато-желтый; длина связи
С — О 0,1475 нм, угол ОСlO 117 °С; ур-ние температурной зависимости давления
пара lgp (мм рт. ст.) = 7,7427 -- 1275,1/T (226-312 К); р-римость
в воде 26,1 г/л (25 °С, 20,68 кПа), раств. в ССl4, НС1О4,
СН3СООН. В индивидуальном состоянии взрывоопасен, при 30-50
°С распад идет с измеримой скоростью, выше 50 С после периода индукции
взрывается. В щелочной среде С1О2 диспропорционирует на и
и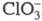 , в
присут. Н2О2 образуется
, в
присут. Н2О2 образуется и выделяется О2. Восстанавливается иодидами, арсенидами, PbO,
H2SO3, аминами до хлорит-иона. СNO2 и
N2O5 образует NO3C1, с NOC1 -NO2C1.
Фторируется посредством AgF2, BrF3 или разб. F2
до C1O2F. Получают СlO2 действием восстановителей
(SO2, NO2, метанол, орг. пероксиды) на подкисленный
р-р хлората щелочного металла, при нагр. смеси хлората с влажной щавелевой
к-той, действием С12 на хлориты. В отличие от остальных X. о.
С1О2 - продукт пром. произ-ва, его используют вместо С12
как экологически более безопасный продукт для отбеливания древесной пульпы,
целлюлозы, синтетич. волокон, для подготовки питьевой и технол. воды, обеззараживания
сточных вод. Раздражает слизистые оболочки, вызывает кашель, рвоту и др.;
ПДК в воздухе рабочей зоны 0,1 мг/м3, ЛД50 140 мг/кг
(крысы, внутрижелудочно).
и выделяется О2. Восстанавливается иодидами, арсенидами, PbO,
H2SO3, аминами до хлорит-иона. СNO2 и
N2O5 образует NO3C1, с NOC1 -NO2C1.
Фторируется посредством AgF2, BrF3 или разб. F2
до C1O2F. Получают СlO2 действием восстановителей
(SO2, NO2, метанол, орг. пероксиды) на подкисленный
р-р хлората щелочного металла, при нагр. смеси хлората с влажной щавелевой
к-той, действием С12 на хлориты. В отличие от остальных X. о.
С1О2 - продукт пром. произ-ва, его используют вместо С12
как экологически более безопасный продукт для отбеливания древесной пульпы,
целлюлозы, синтетич. волокон, для подготовки питьевой и технол. воды, обеззараживания
сточных вод. Раздражает слизистые оболочки, вызывает кашель, рвоту и др.;
ПДК в воздухе рабочей зоны 0,1 мг/м3, ЛД50 140 мг/кг
(крысы, внутрижелудочно).
Перхлорат хлора (цихлоротетраоксид) С12О4,
или СlOС1О3 - светло-желтая жидкость, в кристаллич. состоянии
почти бесцветен (см. Перхлораты).
Триоксид (дихлорогексаоксид) С12О6
- ярко-красная жидкость, в твердом состоянии - оранжевый, при охлаждении
окраска ослабевает. В газе и жидкости молекулы имеют строение О2С1
— О — С1О3, в кристаллах -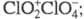 кристаллы моноклинной сингонии (пространств. группа
кристаллы моноклинной сингонии (пространств. группа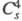 ,
z = 4); давление пара 39,9 Па (0 °С), 133 Па (19 °С). Медленно разлагается
уже при 0-10 °С на С1О2 и О2, выше 20 °С в продуктах
распада появляется С12; с водой реагирует со вспышкой, продукты
гидролиза - НС1О3 и НС1О4. С хлоридами, бромидами,
нитратами образует перхлораты, напр. с NOC1 дает NOC1O4, с N2O5
- NO2C1O4, с А1С13 -СlO2[А1(С1О4)4],
с FeCl3 - ClO2[Fe2(ClO4)7].
При нагр. в вакууме такие комплексы отщепляют С12О6
и превращаются в несольватированные перхлораты А1(С1О4)3,
Fe(ClO4)3. Получают С12О6 р-цией
озона с С1О2 или действием F2 на хлораты металлов.
Применяют для синтеза безводных перхлоратов в лаб. условиях.
,
z = 4); давление пара 39,9 Па (0 °С), 133 Па (19 °С). Медленно разлагается
уже при 0-10 °С на С1О2 и О2, выше 20 °С в продуктах
распада появляется С12; с водой реагирует со вспышкой, продукты
гидролиза - НС1О3 и НС1О4. С хлоридами, бромидами,
нитратами образует перхлораты, напр. с NOC1 дает NOC1O4, с N2O5
- NO2C1O4, с А1С13 -СlO2[А1(С1О4)4],
с FeCl3 - ClO2[Fe2(ClO4)7].
При нагр. в вакууме такие комплексы отщепляют С12О6
и превращаются в несольватированные перхлораты А1(С1О4)3,
Fe(ClO4)3. Получают С12О6 р-цией
озона с С1О2 или действием F2 на хлораты металлов.
Применяют для синтеза безводных перхлоратов в лаб. условиях.
Оксид Cl(VII) (хлорный ангидрид, дихлорогептаоксид)
С12О7 - бесцв. подвижная жидкость, чувствителен к
удару и трению. Молекула имеет строение О3С1 — О — ClO3,
длина связи С1 — О 0,1709 нм, в группах С1О3 - 0,1405 нм, угол
СlOС1 118,6°, ОСlO 115,2°,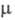 2,40 x 10-30Кл x м; кристаллы моноклинные (пространств. группа
С2/с); ур-ние температурной зависимости давления пара lgp(мм
рт. ст.) = 7,796-1770/Т. Неограниченно раств. в СCl4,
хорошо раств. в НС1О4, РОС13 и т. п. С водой не смешивается,
на границе раздела фаз реагирует с образованием НСlO4, р-ция
сильно экзотермична
2,40 x 10-30Кл x м; кристаллы моноклинные (пространств. группа
С2/с); ур-ние температурной зависимости давления пара lgp(мм
рт. ст.) = 7,796-1770/Т. Неограниченно раств. в СCl4,
хорошо раств. в НС1О4, РОС13 и т. п. С водой не смешивается,
на границе раздела фаз реагирует с образованием НСlO4, р-ция
сильно экзотермична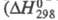 р-ции -211 кДж/моль); разогревание слоя С12О7 может
привести к взрыву. Распад С12О7 в газе на хлор и
кислород идет с измеримой скоростью при 100-120 °С, но при давлении С12О7
выше 13,3 кПа приобретает взрывной характер. Жидкий С12О7
устойчив до 60-70 °С, примесь низших X. о. ускоряет его распад. Для жидкого
С12О7 характерны р-ции с образованием ковалентных
соед. с группой — С1О3. С NH3 в ССl4 образует
NH4HNC1O3 и NH4C1O4, с алкиламинами
-соотв. RHNC1O3 и R2NC1O3, с SbF5
- SbOF3 и FC1O3, с N2O5 в ССl4
NO2C1O4. Используя С12О7, можно
синтезировать орг. перхлораты из спиртов. Получают С12О7
действием Р2О5 или олеума на хлорную к-ту или электролизом
р-ра НС1О4 на Pt-электродах ниже 0 °С (С12О7
накапливается в анодном пространстве). Чистый С12О7
можно получить также при нагр. в вакууме нек-рых перхлоратов, напр. Nb(ClO4)5,
МоО2(СlO4)2.
р-ции -211 кДж/моль); разогревание слоя С12О7 может
привести к взрыву. Распад С12О7 в газе на хлор и
кислород идет с измеримой скоростью при 100-120 °С, но при давлении С12О7
выше 13,3 кПа приобретает взрывной характер. Жидкий С12О7
устойчив до 60-70 °С, примесь низших X. о. ускоряет его распад. Для жидкого
С12О7 характерны р-ции с образованием ковалентных
соед. с группой — С1О3. С NH3 в ССl4 образует
NH4HNC1O3 и NH4C1O4, с алкиламинами
-соотв. RHNC1O3 и R2NC1O3, с SbF5
- SbOF3 и FC1O3, с N2O5 в ССl4
NO2C1O4. Используя С12О7, можно
синтезировать орг. перхлораты из спиртов. Получают С12О7
действием Р2О5 или олеума на хлорную к-ту или электролизом
р-ра НС1О4 на Pt-электродах ниже 0 °С (С12О7
накапливается в анодном пространстве). Чистый С12О7
можно получить также при нагр. в вакууме нек-рых перхлоратов, напр. Nb(ClO4)5,
МоО2(СlO4)2.
Известен ряд хлоркислородных свободных
радикалов, полученных в разл. низкотемпературных матрицах и исследованных
преим. методом ЭПР,- СlО3, СlОО, СlСlО, а также малостабильный
сесквиоксид Сl2О3, распадающийся при -50 - 0 °С и
имеющий, вероятно, структуру хлората хлора СlOСlO2. Термически
устойчивый радикал СlO (длина связи С1 — О 0,1569 нм,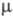 4,133 Кл x м,
4,133 Кл x м,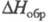 101,6 кДж/ моль) -промежут. продукт окисления углеводородов хлорной к-той
и X. о., распада всех X. о. и др. хлоркислородных соед., а также р-ции
озона с атомарным хлором в стратосфере.
101,6 кДж/ моль) -промежут. продукт окисления углеводородов хлорной к-той
и X. о., распада всех X. о. и др. хлоркислородных соед., а также р-ции
озона с атомарным хлором в стратосфере.
Лит.: Никитин И. В., Химия кислородных соединений галогенов, М., 1986.
В.Я.Росоловский.

