Нежесткие молекулы
НЕЖEСТКИЕ МОЛЕКУЛЫ, молекулы,
у к-рых малые изменения энергии или пространств. расположения атомных ядер (геом.
конфигурации) приводят к существенным, подчас качеств., изменениям св-в. Нежесткость
присуща, как правило, лишь отдельным состояниям молекулы, тогда как при переходе
к др. состояниям она отсутствует.
Понятие "Н. м."
возникло в связи с тем, что квантовомех. описание мол. систем проводится в рамках
адиабатического приближения традиционно, на основе след. модели: движение
электронов и ядер адиабатически разделяется; поведение каждого из электронов
определяется в одноконфигурац. приближении соответствующей мол. орбиталью (напр.,
в приближении самосогласованного поля; см. Молекулярных орбиталей методы);
для представления движения ядер их рассматривают как систему связанных гармонич.
осцилляторов (или ангармонич. осцилляторов Морса), совершающих малые колебания
вблизи положения равновесия; вся молекула к тому же вращается как единое жесткое
целое (жесткий ротатор). Если эта модель приемлема для описания молекулы и все
отклонения от нее при переходе к точному описанию м. б. учтены как малые поправки
(малые возмущения), молекулу наз. ж е с т к о й. Для "жесткой" модели
характерна единств. равновесная ядерная конфигурация, к-рой отвечает четко выраженный
минимум потенц. энергии, и малые (по сравнению с межъядерными расстояниями)
амплитуды колебаний ядер. Если молекула обладает неск. устойчивыми равновесными
ядерными конфигурациями, жесткую модель применяют в тех случаях, когда энергия
активации перехода между этими конфигурациями (потенц. барьер) превышает при
обычных т-рах ~100 кДж/моль.
Как правило, жесткая модель
удовлетворительно описывает лишь низшие колебательно-вращат. энергетич. уровни
осн. электронного состояния молекул большинства хим. соединений. Симметрия жестких
молекул определяется точечной группой симметрии равновесной ядерной конфигурации,
по неприводимым представлениям к-рой классифицируются состояния таких молекул.
Физ. методы (газовая электронография, ЯМР и др.) позволяют определять точечную
группу симметрии и параметры равновесной конфигурации.
К жестким молекулам относят как простые молекулы, напр. СО2, ВСl3,
SO3, CH4, SF6, так и нек-рые сложные мол. системы,
напр. бензол, адамантан, карбораны. Нарушения применимости жесткой модели наз.
э ф ф е кт а м и н е ж е с т к о с т и, а молекула в соответствующем состоянии
считается н е ж е с т к о й. Следует отметить, что повышение точности эксперим.
исследований приводит, как правило, к расширению числа Н.м. Иногда выделяют
и промежут. случаи-т. наз. полужесткие молекулы. Н.м. могут обладать неск. равновесными
ядерными конфигурациями. Различают структурно-нежесткие и электронно-нежесткие
молекулы, в зависимости от того, для какой из подсистем молекулы - ядер или
электронов-существенно отклонение от жесткой модели. Для структурно-нежестких
молекул существенно, что колебания ядер по форме отличаются от гармонических
либо характерных для ангармонич. осцилляторов Морса; в частности, амплитуды
колебаний велики и сравнимы по порядку величины с длинами связей. Если при малых
изменениях равновесной геом. конфигурации ядер молекулы происходит резкая перестройка
электронной конфигурации, говорят об электронной нежесткости.
Структурно-нежесткие
молекулы характеризуются тем, что потенциал, поле к-рого определяет колебания
ядер, слабо меняется вдоль одной или неск. пространств. координат. Движения
по этим координатам наз. нежесткими движениями. Колебания ядер происходят с
большой амплитудой, а осн. частота колебаний вдоль "нежесткой" координаты
обычно гораздо меньше частот "жестких" валентных и деформац. колебаний
и может приближаться даже к характерным величинам вращат. частот. При переходе
от одних колебат. состояний к другим заметно меняется средняя геом. конфигурация
молекулы. Достаточно малые внеш. воздействия, обусловленные, напр., окружением
молекулы в конденсир. фазе, заметно меняют вероятность распределения ядер в
разл. областях пространства. Жесткие молекулы, наоборот, сохраняют свою геом.
конфигурацию при таких воздействиях.
Отдельные классы структурно-нежестких
молекул были известны давно; напр., молекулы со слабо заторможенным внутр. вращением
(см. Внутреннее вращение молекул), а также молекулы, изомеры к-рых переходят
друг в друга при тепловом движении, т. е. при энергиях возбуждения порядка неск.
RT(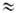 2,5
кДж/моль при 300 К) (T-абс. т-ра, R-газовая постоянная), так что
равновесие между такими изомерами (конформерами) устанавливается быстро даже
при сравнительно низких т-рах. Так, в молекуле этана барьер внутр. вращения
равен ~ 12 кДж/моль, а в молекуле метил-германа - всего лишь ~5кДж/моль. При
таутомерных превращ. барьер также подчас настолько мал, что равновесие между
таутомерами устанавливается очень быстро и выделить их в изолир. состоянии оказывается
невозможным (см. Таутомерия).
2,5
кДж/моль при 300 К) (T-абс. т-ра, R-газовая постоянная), так что
равновесие между такими изомерами (конформерами) устанавливается быстро даже
при сравнительно низких т-рах. Так, в молекуле этана барьер внутр. вращения
равен ~ 12 кДж/моль, а в молекуле метил-германа - всего лишь ~5кДж/моль. При
таутомерных превращ. барьер также подчас настолько мал, что равновесие между
таутомерами устанавливается очень быстро и выделить их в изолир. состоянии оказывается
невозможным (см. Таутомерия).
Н.м. являются соли кислородсодержащих
к-т и комплексные галогениды металлов, напр. RbNO3, KClO4,
LiAlF4 и т. п. Так, у молекул галогенидов в газовой фазе имеется,
как правило, жесткий остов типа AlF4, вокруг к-рого относительно
свободно может перемещаться остаток, напр. Li. Хим. связь в таких соед. по характеру
очень близка к ионной. На поверхности потенциальной энергии (ППЭ) того
или иного электронного состояния этих молекул имеется обычно неск. эквивалентных
(или почти эквивалентных) минимумов, отделенных друг от друга невысокими барьерами;
так, у LiAlF4 имеется 4 минимума, отвечающих расположению атома Li
над гранями тетраэдра AlF4. Такого рода молекулы наз. политопными.
К числу политопных молекул относят и молекулы типа PF5, на ППЭ к-рой
эквивалентные минимумы отвечают конфигурации треугольной бипирамиды симметрии
D3h. Эти конфигурации при определенных колебаниях переходят
друг в друга: молекула как бы поворачивается (с сохранением вращат. момента
импульса) от одной конфигурации к другой, эквивалентной первой. Такое колебат.
движение наз. псевдовращениeм Берри, а молекулы, у к-рых оно проявляется,
иногда наз. стереохимически нежесткими
(см. Политопные перегруппировки). К движениям с большой амплитудой и
переходами между эквивалентными минимумами относится также инверсия пирамидальных
молекул, напр., аммиака и аминов.
У молекул типа LiNC нет
эквивалентных минимумов, однако тот желоб на ППЭ, вдоль к-рого совершает нежесткие
колебания ядро Li, очень пологий: вдоль этого желоба конфигурации на ППЭ отвечает
абс. минимум; кроме того, имеются неглубокие минимумы для Т-образной конфигурации
и для почти линейной конфигурации LiCN на ~3,1 и 9,7 кДж/моль выше абс. минимума
соответственно. Частота деформац. колебания составляет вблизи конфигурации LiNC
ок. 100 см-1, т.е. 1,2 кДж/моль. По мере увеличения колебат. возбуждения
молекула меняет свою среднюю геом. конфигурацию: если в осн. состоянии это линейная
конфигурация LiNC, то при переходе в более высокие колебат. состояния конфигурация
становится все более изогнутой. У молекулы RbCN минимум на ППЭ отвечает треугольной
конфигурации, тогда как линейным конфигурациям RbCN и RbNC (с небольшим локальным
минимумом) отвечают более высокие энергии (на 500 и 2000 см-1 соотв.).
Если движения ядер с большими
амплитудами происходят в области одного минимума на ППЭ, молекулу наз. л о к
а л ь н о-н е ж е с т к о й. Если же при таких движениях происходят перемещения
атомов или групп атомов из одной области пространства в другую или даже перестройка
скелета молекулы (напр., при таутомерных превращ.), молекулы наз. г л о б а
л ь н о-н е ж е с т к и м и. У глобально-нежестких молекул на ППЭ обычно имеется
неск. близких по энергии минимумов, разделенных низкими (порядка энергии теплового
движения) потенц. барьерами.
Если в нек-ром нестационарном
состоянии молекулы волновая ф-ция, описывающая движение ядер, локализована у
одного из минимумов ППЭ, то при послед. эволюции этого состояния во времени
рано или поздно возникает состояние, также нестационарное, в к-ром волновая
ф-ция будет локализована у др. минимума. Время, к-рое система проводит в одном
из минимумов (или время, за к-рое происходит такой переход), обычно наз. временем
жизни в этом минимуме. Чем выше барьеры между минимумами и чем они шире, тем
больше время жизни мол. системы в соответствующем минимуме ППЭ. У структурно-нежестких
молекул времена жизни в отдельных минимумах, отвечающих нежестким движениям,
обычно малы. Так, у PF5 частота перехода из одной конфигурации симметрии
D3h в другую, ей эквивалентную, равна 105
Гц, т. е. время жизни в одном из минимумов составляет 10-5 с. Поэтому
метод ЯМР, характеристич. время измерений к-рого составляет от 10-1
до 10-9 с, не позволяет различить неэквивалентные аксиальные и экваториальные
атомы F, тогда как электро-нографич. эксперимент с характеристич. временем измерений
порядка 10-20 с допускает обнаружение их различий: равновесное расстояние
между ядрами Re (Р — Faкc) = 0,1577 нм, Re(P
— Fэкв) = 0,1534 нм. Малые времена жизни характерны и для оптич.
изомеров хиральных аминов, к-рые при комнатной т-ре оптически неактивны именно
из-за быстрого превращ. одного изомера в другой и обратно (каждый из оптич.
изомеров также отвечает нестационарному состоянию с большим или меньшим временем
жизни).
Симметрия структурно-нежестких
молекул описывается т. наз. перестановочно-инверсионной группой, включающей
группу перестановок тождеств. ядер и группу инверсии, состоящую из тождеств.
операции и операции инверсии. Число элементов перестановочно-инверсионной группы
обычно весьма велико, однако если в молекуле выделить жесткие фрагменты, напр.
метильные группы, аминогруппы, то это число значительно сокращается.
Электронно-нежесткие
молекулы отличаются относительно резкими изменениями электронных св-в вблизи
тех геом. конфигураций ядер, где происходит переход от одних электронных конфигураций,
доминирующих в волновой ф-ции молекулы, к другим, т.е. происходит существ. изменение
электронного распределения. Так, в основном состоянии у
двухатомных молекул типа LiF, AlO и др. для равновесной конфигурации и вблизи
нее характерен ионный тип связи: Li+ F-, A12+
O2- и т.п. Однако при увеличении межъядерного расстояния R, подчас
достаточно близко от равновесного расстояния Re, электронная
конфигурация меняется, напр., с переходом к ковалентному типу связи и в конечном
итоге-с переходом к диссоциац. пределу, отвечающему взаимод. двух нейтральных
подсистем Li + F, Al + О и т. д. В тех областях пространства, где происходит
такая смена доминирующей электронной конфигурации, наблюдается резкое изменение
зависимости от R электронного диполь-ного момента me(R),
поляризуемости a(R), их производных по R и др. электронных
св-в (см. рис.). Это приводит и к изменениям св-в, усредненных по колебаниям
ядер, напр. к резким изменениям средних для каждого колебат. состояния дипольного
момента, поляризуемости, а также вероятностей квантовых переходов. Так, в спектрах
могут "пропадать" отдельные линии и полосы из-за очень малых величин
соответствующих вероятностей переходов, поскольку эти вероятности перехода пропорциональны
квадрату модуля матричных элементов дипольного момента перехода (см. Квантовые
переходы). У мн. молекул существует неск. областей перестройки доминирующей
электронной конфигурации, особенно в возбужденных электронных состояниях, что
приводит к значит. усложнению поведения молекулы в таких состояниях, особенно
при хим. превращениях.
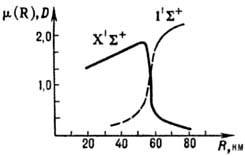
Зависимость дипольного
момента m (в дебаях D) молекулы LiF
от межъядерного расстояния R для основного 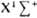 состояния и
первого возбужденного
состояния и
первого возбужденного 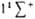 состояния того же типа симметрии.
состояния того же типа симметрии.
С электронной нежесткостью
часто связаны Яна - Теллера эффекты, когда высокосимметричная конфигурация
А ядер, приводящая к вырожденному электронному состоянию, оказывается конфигурацией
локального максимума на ППЭ молекулы, тогда как минимумам на ППЭ отвечают конфигурации
ядер В1, В2, ..., Вn с более низкой
симметрией, переходящие друг в друга при операциях симметрии конфигурации А,
причем в этих минимумах электронные конфигурации уже иные, чем в исходном вырожденном
состоянии. Такие минимумы к тому же часто бывают разделены невысокими барьерами,
что создает благоприятные условия для проявления структурной нежесткости у соответствующих
молекул.
Нежесткость молекул проявляется
и в состояниях сильного вращат. возбуждения, особенно у высокосимметричных молекул,
когда качественно изменяется распределение по энергии вращат. состояний. Так,
у молекул типа сферич. волчка (СН4, GeH4 и т. п.) при
больших значениях вращат. квантового числа J (порядка 40-100) энергетич.
спектр вращат. уровней имеет "кластерную" структуру: он состоит
из системы "кластеров", включающих по 8 очень близко расположенных
уровней (на расстоянии 10-4 см-1 и менее), тогда как сами
"кластеры" удалены друг от друга на значительно большие расстояния
(порядка 10-1 см-1 и более). При нек-рых значениях
J, зависящих от конкретной молекулы, кластерная структура (а вместе с
ней и структура вращат. спектров) резко меняется: происходит, напр., перестройка
и переход к кластерам, включающим по 6 уровней ("вращат. фазовые переходы").
Такого типа нежесткость часто наз. вращательной.
Нежесткость отдельных видов
движения в той или иной степени присуща всем молекулам, начиная с Н2
(в возбужденных электронных состояниях) и кончая сложными белковыми молекулами,
у к-рых одновременно проявляются разл. типы нежесткости: почти своб. вращение
вокруг отдельных связей, слабые изменения расстояний между отдельными фрагментами,
допускающие, напр., интеркаляцию
др. молекул, в частности антибиотиков и т. д. Проявления нежесткости молекул
наблюдаются и на макроскопич. уровне, напр. в виде необычной температурной зависимости
теплоемкости или в виде необычно высоких значений энтропии, в т.ч. энтропии
хим. р-ций с участием Н.м. В осн. эти проявления связаны со структурной нежесткостью,
однако при хим. р-циях весьма существенна и электронная нежесткость.
Лит.: Жилинский
Б. И., Истомин В. А., Степанов Н.Ф., Колебательно-вращательные состояния нежестких
молекул, в сб.: Современные проблемы физической химии, т. 11, М., 1979, с. 259-304;
Пирсон Р., Правила симметрии в химических реакциях, пер. с англ., М., 1979;
Маркин О.П., Болдырев А. И., в кн.: Итоги науки и техники, сер. Неорганическая
химия, т. 8, М., 1980; Байкер Ф. Р., Симметрия молекул и молекулярная спектроскопия,
пер. с англ., М., 1981; Symmetries and properties of non-rigid molecules, ed.
by J. Maruani, J. Serre, Amst. 1983. Н. Ф. Степанов.

