Графита соединения
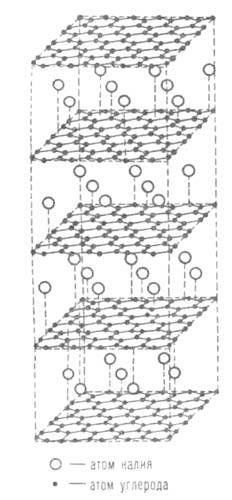
Кристаллич. решетка С8К; темные кружки -атомы углерода, светлые-калия.
Соед. со щелочными металлами могут иметь составы С8М, С16М, С24М, С36М, С40М, С64М. Металл в решетке находится в виде атома; при его ионизации происходит перенос электронов в зону проводимости графита. Структура С8К представлена на рисунке. У этого соед. атомы металла располагаются над центрами гексаген, колец из атомов углерода. В соед. С16М атомы металла расположены так же, но только между каждой парой слоев графита. Аналогично построены и др. соединения. В случае С64М один ме-таллич. слой приходится на восемь углеродных.
В отличие от др. щелочных металлов, Na образует соед. с большим избытком
углерода: из прир. графита получены C120Na, C64Na,
C36Na, из искусственно полученного-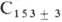 Na. По уменьшению деформирующего действия на решетку графита при образовании
слоистых соед. щелочные металлы располагаются в ряд: Cs, Rb, К, Na, Li.
Соед. с графитом образуют также др. металлы-Ва, Sr, Zn, Cd и многие РЗЭ.
В соед. с галогенами происходит перенос электронов из зоны проводимости
графита к атомам галогена, в результате чего образуются положительно заряженные
дырки. наиб. известны бромсодержащие Г. с., напр. С8Вr. Синтезированы
соед. с фтором состава CF0,676-CF0,998, C2F
и C4F.
Na. По уменьшению деформирующего действия на решетку графита при образовании
слоистых соед. щелочные металлы располагаются в ряд: Cs, Rb, К, Na, Li.
Соед. с графитом образуют также др. металлы-Ва, Sr, Zn, Cd и многие РЗЭ.
В соед. с галогенами происходит перенос электронов из зоны проводимости
графита к атомам галогена, в результате чего образуются положительно заряженные
дырки. наиб. известны бромсодержащие Г. с., напр. С8Вr. Синтезированы
соед. с фтором состава CF0,676-CF0,998, C2F
и C4F.
Получены Г. с. с кислородсодержащими к-тами, напр. C24HSO4- *H2SO4 (гидросульфат графита). H2SO4 внедряется в решетку графита в виде ионов HSO4 или молекул. Известны соед. с HF, напр. C+24HF-2 *2H2F2.
Весьма многочисленны соед. с галогенидами (напр., с А1С13, FeCl3, ZrCl4, UC14, МоС15, MoF6, BrF3, IC1), оксига-логенидами (СrО2С12, CrO2F2, UO2C12, XeOF2), оксидами и сульфидами металлов. Их часто наз. "молекулярными комплексами", т. к. они образуются при внедрении галогенидов в решетку графита в виде молекул. Из соед. с галогенидами металлов наиб. изучено соед. с FeCl3, в к-ром содержание хлорида может достигать 56%; при этом возможные для заполнения слои заняты только на 92%. В случае А1С13 соед. имеет ф-лу С+m[АlС14 + nАlС13], где соотношение m:(n+l) составляет 1:9, 1:18 или 1:36. Сульфид или хлорид металла с переменной валентностью при внедрении в графит приобретает более высокую степень окисления.
Свойства. Соед. с небольшим содержанием внедрившегося в-ва имеют черный цвет и по внеш. виду мало отличаются от исходного графита. По мере увеличения содержания их цвет меняется сначала на сине-голубой, затем на желто-оранжевый.
Наиб. интересное св-во Г. с.- высокая электрич. проводимость, приближающаяся к проводимости Си или Ag, a в ряде случаев даже превышающая ее в 2-5 раз. Макс. проводимость характерна для соед. с акцепторами электронов, напр. с IC1. Так, электрич. проводимость вдоль оси а: для С82IС11,08 0,9*10-3 Ом-1*m-1; для C16,3IC11,1, 2,8*10-3 Ом-1 *м-1; для С33,0IС11,1 1,3*10-3 Ом-1*м-1. Эти зна-
чения в 70 раз превышают электрич. проводимость исходного пиролитич. графита и близки к проводимости Аи. С понижением т-ры электрич. проводимость Г. с. увеличивается. Соед. с К, Rb и Cs обладают сверхпроводящими св-вами.
Соед. со щелочными металлами не разлагаются при комнатной т-ре в инертной атмосфере; легко окисляются; взаи-мод. с Н2 и N2. При высоких т-рах металл может испаряться. Хим. способами полностью удалить металл из соед. не удается. При повыш. т-рах большинство Г. с. отличается высокой хим. активностью. При термич. или хим. разложении, к-рое может протекать весьма бурно, слоистая структура сохраняется без изменений. При гидролизе из этих соед. выделяется только Н2.
Особенность Г. с. с галогенами, нек-рыми галогенидами металлов и др.-способность удерживать часть внедрившихся атомов или молекул даже при высоких т-рах. Такие соед. наз. "остаточными", они устойчивы даже при нагревании в нейтральных средах и в вакууме до 1200-1500 °С; предполагают, что внедрившиеся атомы и молекулы закрепляются на дефектах кристаллической решетки графита.
Получение. Г. с. образуются, как правило, при нагревании графита с внедряющимися в-вами, напр. с хлоридами металлов-при 230-280 °С, с щелочными металлами-при 300 °С и выше. С бромом графит реагирует при комнатной т-ре. В нек-рых случаях требуется "катализатор" (напр., С12), роль к-рого сводится к обмену электронами с реагентами в случае отсутствия такой способности (по отношению к графиту) у внедряющегося в-ва. Катализаторы входят в состав Г. с. Так, при образовании соед. с А1С13 один атом С1 приходится на три молекулы хлорида, в случае InС13 или GdCl3-Ha шесть молекул хлорида.
Наиб. подробно изучено образование слоистых соединений с конц. H2SO4 в присут. окислителей-HNO3, CrO3, КМnО4 и др. Гидросульфат графита получают в виде достаточно крупных образцов в сравнительно больших масштабах, используя анодное окисление пиролитич. графита. Интенсивно изучается синтез слоистых Г. с. с галогенидами при давлениях до 10 МПа. В этом случае следует ожидать получения соед. с т. наз. невнедряющимися в графит галогенидами, напр. с SeCl4, PC15, AsCl3. Такие соединения м. б. основой новых неорг. материалов.
Применение. Пром. применение Г. с. очень быстро расширяется. Соединения с к-тами используют в хим. машиностроении в кач-ве антифрикционных материалов и химически стойких прокладок. На основе соединений с Li создаются батареи высокой емкости. Соединения с галогенами применяют в орг. синтезе в кач-ве мягких фторирующих и хлорирующих агентов, с фтором-как твердую смазку, материал катодов (в хим. источниках тока) и щеток для электродвигателей. Из смесей Г. с. с медью или алюминием изготавливают материалы, к-рые вследствие их малой плотности, высокой электрич. проводимости, сравнительной дешевизны применяют для изготовления проводов. Высокая электрич. проводимость Г. с. позволяет применять их вместо графита в кач-ве наполнителей пластмасс. Многие соед. являются катализаторами, в т.ч. полимеризации, изомеризации; соед. К, Rb и Cs катализируют конверсию ортоводорода в параводород. См. также Интеркалаты.
Лит.: Новиков Ю. Н., Вол ьпин М.Е., "Успехи химии", т. 40, № 9, 1971, с. 1568-92; Коллонг Р., Нестехиометрия, пер. с франц., М., 1974; Свойства конструкционных материалов на основе углерода. Справочник, под ред. В. П. Сосе-дова, М., 1975. В. Н. Костиков.

