Валериановые кислоты
ВАЛЕРИАНОВЫЕ КИСЛОТЫ С4Н9СООН, мол. м. 102,13. В статье рассмотрены к-ты, содержащие бутильный остаток, связанный с группой СООН.
Валериановая (пентановая) к-та СН3(СН2)3СООН
(В.к.) - бесцв. жидкость; т. пл. -34,5°С, т. кип. 185,4°С, 93,5-94°С/21
мм рт. ст.; d420 0,9459, nD20
1,41.00;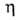 2,359 мПа*с (15°С);
2,359 мПа*с (15°С); Hoобр
- 548,9 кДж/моль,
Hoобр
- 548,9 кДж/моль,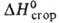 -2853,4 кДж/моль; К 1,147*10-5 (20°С); р-римость в воде
4,97% (25 °С). Образует бинарные азеотропные смеси с многими в-вами, напр.
с бромбензолом (3,5% В.к.; т. кип. 155,6°С). Соли и эфиры В. к. наз. валератами.
Содержится в продуктах перегонки древесины, бурого угля и др. В пром-сти
получают гидроформилированием 1-бутена с послед. окислением образующегося
альдегида; окислением амилового спирта. Наряду с бутилвалератом получается
при обработке бутанола СО в присут. NiI2 и Nal или никеля Ренея
в водном р-ре при 340 °С и 37,5 МПа. Эфиры В. к., обладающие фруктовым
и цветочным запахом (напр., изомилвалерат), - ароматизирующие в-ва для
пищ. продуктов, душистые в-ва в парфюмерии; используют также как р-рители,
сырье в произ-ве лек. в-в.
-2853,4 кДж/моль; К 1,147*10-5 (20°С); р-римость в воде
4,97% (25 °С). Образует бинарные азеотропные смеси с многими в-вами, напр.
с бромбензолом (3,5% В.к.; т. кип. 155,6°С). Соли и эфиры В. к. наз. валератами.
Содержится в продуктах перегонки древесины, бурого угля и др. В пром-сти
получают гидроформилированием 1-бутена с послед. окислением образующегося
альдегида; окислением амилового спирта. Наряду с бутилвалератом получается
при обработке бутанола СО в присут. NiI2 и Nal или никеля Ренея
в водном р-ре при 340 °С и 37,5 МПа. Эфиры В. к., обладающие фруктовым
и цветочным запахом (напр., изомилвалерат), - ароматизирующие в-ва для
пищ. продуктов, душистые в-ва в парфюмерии; используют также как р-рители,
сырье в произ-ве лек. в-в.
Изовалериановая (3-метилбутановая, (5-метилмасляная) к-та (СН3)2СНСН2СООН
(И.к.)-бесцв. жидкость; т. пл. -29,3°С, т. кип. 176,5°С, 99,5°С/37 мм рт.
ст.; d415 0,9308, nD15 1,4030;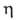 2,731
МПа*с (15°С);
2,731
МПа*с (15°С);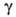 0,024
Н/м (30 °С);
0,024
Н/м (30 °С);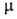 3,03*10-30 Кл*м;
3,03*10-30 Кл*м;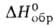 -561,5 кДж/моль,
-561,5 кДж/моль,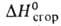 - 2840,8 кДж/моль; К 1,216*10-5 (60°С); раств. в воде
(4,2 г в 100 мл), этаноле, эфире, хлороформе. Соли и эфиры И.к. наз. изовалератами,
напр. этилизовалерат (т. пл. 134,1°С; d420 0,8656,
nD20 1,3692; р-римость в воде 0,17%; содержится в
ананасах), изоамилизовалерат (жидкость; т. кип. 73-76°С/14 мм рт. ст.;
d420 0,8812, nD20
1,4108; в воде раств. плохо).
- 2840,8 кДж/моль; К 1,216*10-5 (60°С); раств. в воде
(4,2 г в 100 мл), этаноле, эфире, хлороформе. Соли и эфиры И.к. наз. изовалератами,
напр. этилизовалерат (т. пл. 134,1°С; d420 0,8656,
nD20 1,3692; р-римость в воде 0,17%; содержится в
ананасах), изоамилизовалерат (жидкость; т. кип. 73-76°С/14 мм рт. ст.;
d420 0,8812, nD20
1,4108; в воде раств. плохо).
И.к. содержится в корне валерианы лекарственной, из к-рого ее и получают отгонкой с водяным паром, а также в чайном листе, эфирных маслах нек-рых цитрусовых и др. Синтезируют ее окислением изоамилового спирта, напр.: электролитич. способом в р-ре H2SO4 с добавкой MnSO4 на аноде, изготовленном из РbО2, при 20°С; при нагр. на воздухе с NaOH + КОН (в соотношении 2:1) и небольшим кол-вом Н2О при 285-295°С или с NaOH в присут. основного карбоната меди CuCO3*Cu(OH)2*0,5Н2О при 140°С. Вместе с пивалиновой к-той получается карбонилированием изобутилена при 250°С и 20 МПа [кат. - Ni(СО)4 и NiI2]. И.к. применяют в произ-ве валидола, бромизовала, корвалола, валокордина и др. лек. в-в, фруктовых эссенций и душистых в-в в парфюмерии.
Метилэтилуксусная (2-метилбутановая,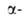 метилмасляная)
к-та СН3СН2СН(СН3)СООН (М.к.) - бесцв.
жидкость, оптически активна. (+)-Изомер-т. кип. 86,5-87,5°С/26 мм рт. ст.;d425
0,9313, nD20 1,4058;
метилмасляная)
к-та СН3СН2СН(СН3)СООН (М.к.) - бесцв.
жидкость, оптически активна. (+)-Изомер-т. кип. 86,5-87,5°С/26 мм рт. ст.;d425
0,9313, nD20 1,4058;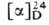 + 35,56° (неразбавленная к-та). Получают (+ ) - M. к. расщеплением рацемата
с помощью цинхонидина. Содержится в эфирных маслах, напр. лавандовом. (-)-Изомер
- т. кип. 71-72°С/12 мм рт. ст., 64°С/2мм рт. ст; d425
0,9340, nD25 1,4038;
+ 35,56° (неразбавленная к-та). Получают (+ ) - M. к. расщеплением рацемата
с помощью цинхонидина. Содержится в эфирных маслах, напр. лавандовом. (-)-Изомер
- т. кип. 71-72°С/12 мм рт. ст., 64°С/2мм рт. ст; d425
0,9340, nD25 1,4038;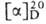 —24° (водный р-р; концентрация 0,9 мг/л). Синтезируют (—) - М. к. окислением
2-метил-1-бутанола действием КМnО4 в водно-щелочном р-ре или
К2Сr2О7 в среде H2SO4.
При окислении (— )-изомера М. к. действием КМnО4 в водно-щелочном
р-ре получается 2-ги-дрокси-2-метилмасляная к-та. Рацемат М. к.-т. пл.
— 48 оС, т. кип. 176,5°С, 88°С/20мм рт. ст.; d420
0,9361, nD20 1,4060;
—24° (водный р-р; концентрация 0,9 мг/л). Синтезируют (—) - М. к. окислением
2-метил-1-бутанола действием КМnО4 в водно-щелочном р-ре или
К2Сr2О7 в среде H2SO4.
При окислении (— )-изомера М. к. действием КМnО4 в водно-щелочном
р-ре получается 2-ги-дрокси-2-метилмасляная к-та. Рацемат М. к.-т. пл.
— 48 оС, т. кип. 176,5°С, 88°С/20мм рт. ст.; d420
0,9361, nD20 1,4060;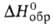 -557,3 кДж/моль,
-557,3 кДж/моль,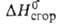 -2845
кДж/моль. Синтезируют декарбоксилированием метилэтилмалоновой к-ты, карбонилированием
втор-бутанола действием Ni(CO)4 в присут. NiCl2 и
соляной к-ты при 300 °С и 4 МПа или пропусканием смеси втор-бутанола и
СО над NiI2 на силикагеле при 230°С и 21 МПа, а также гидрокарбонилированием
1-бутена в разб. уксусной к-те в присут. Ni(CO)4 (при этом образуется
и валериановая к-та). Применяется рацемич. М.к. в произ-ве пластификаторов,
синтетич. смазок, лек. в-в, как экстрагент меркаптанов из углеводородов
и стабилизатор виниловых полимеров.
-2845
кДж/моль. Синтезируют декарбоксилированием метилэтилмалоновой к-ты, карбонилированием
втор-бутанола действием Ni(CO)4 в присут. NiCl2 и
соляной к-ты при 300 °С и 4 МПа или пропусканием смеси втор-бутанола и
СО над NiI2 на силикагеле при 230°С и 21 МПа, а также гидрокарбонилированием
1-бутена в разб. уксусной к-те в присут. Ni(CO)4 (при этом образуется
и валериановая к-та). Применяется рацемич. М.к. в произ-ве пластификаторов,
синтетич. смазок, лек. в-в, как экстрагент меркаптанов из углеводородов
и стабилизатор виниловых полимеров.
Пивалиновая (триметилуксусная, неопентановая) к-та (СН3)3ССООН
(П.к.)-т. пл. 35,7°С, т. кип. 164,15°С, 77-78°С/20мм рт.ст.; d2040
0,905, nD25 1,4030;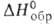 - 565,7 кДж/моль,
- 565,7 кДж/моль,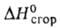 - 2836,6 кДж/моль;
- 2836,6 кДж/моль;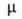 5,7*10-30 Кл*м; К 0,732*10-5 (60°С); р-римость
в 100 г воды 2,2 г (20°С). Р-ции П. к. осложнены стерич. препятствиями,
связанными с экранированием карбоксильной группы СН3-группами.
Напр., П. к. труднее этерифицируется, чем другие В.к.; эфиры ее более устойчивы
при гидролизе и окислении. При окислении Н2О2 в присут.
FeSO4 в водном р-ре H2SO4 П. к. превращается
в 2,2,5,5-тетраметиладипиновую к-ту НООСС(СН3)2СН2СН2С(СН3)2СООН,
хлорируется при облучении УФ-светом (
5,7*10-30 Кл*м; К 0,732*10-5 (60°С); р-римость
в 100 г воды 2,2 г (20°С). Р-ции П. к. осложнены стерич. препятствиями,
связанными с экранированием карбоксильной группы СН3-группами.
Напр., П. к. труднее этерифицируется, чем другие В.к.; эфиры ее более устойчивы
при гидролизе и окислении. При окислении Н2О2 в присут.
FeSO4 в водном р-ре H2SO4 П. к. превращается
в 2,2,5,5-тетраметиладипиновую к-ту НООСС(СН3)2СН2СН2С(СН3)2СООН,
хлорируется при облучении УФ-светом (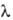 =
365,5 нм) в 3-хлор-2,2-диметилпропионовую к-ту С1СН2С(СН3)2СООН,
при взаимод. с РС13, РС15, SOC12 или СОС12
образуется пивалоилхлорид. Соли и эфиры П. к. наз. пивалатами, напр. этилпивалат
(т. пл. 89,5 °С, т. кип. 119°С).
=
365,5 нм) в 3-хлор-2,2-диметилпропионовую к-ту С1СН2С(СН3)2СООН,
при взаимод. с РС13, РС15, SOC12 или СОС12
образуется пивалоилхлорид. Соли и эфиры П. к. наз. пивалатами, напр. этилпивалат
(т. пл. 89,5 °С, т. кип. 119°С).
В пром-сти П. к. получают карбонилированием изобутилена в присут. HF и Н2О при 40-60°С и 5 МПа; выход 95%. С хорошими выходами м. б. синтезирована таким же способом из бутанола или трет-бутанола (кат. - НВF4*Н2О) в среде H2SO4. П. к. применяют в произ-ве лек. в-в, теплостойких смазок, гербицидов и аттрактантов; к-та и ее Li-соль повышают октановое число моторных топлив. Для защиты древесины м. б. использован пивалат Sn. Эфиры П. к. с бутиловыми спиртами - ароматизирующие в-ва для пищ. продуктов (фруктовый, цветочный или винный запах), эфиры с полиолами-пластификаторы.
Лит.: Ullmans Encyklopadie, 4 Aufl., Bd9,Weinheim, 1975, S. 142-44:
Kirk-Othmer encyclopedia, 3 ed., v. 4, N. Y.-[a.o.J, 1978, p. 864-71. И.В.
Хвостов.

