Марганец
Свойства. Компактный М. - серебристо-белый металл. Известно 4 кубич. кристаллич. модификации М.: ниже 710°С устойчива a-форма (а = 0,89125 нм, z = 58, пространств. группа I43m, плотн. 7,44 г/см3), при 710-1090°С - b-форма (а = 0,6300 нм, z = 20, пространств. группа P413, плотн. 7,29 г/см3), при 1090-1137°С - g-форма (а = 0,38550 нм при 1100°С, z = 4, пространств. группа Fm3m, плотн. 6,37 г/см3), выше 1137°С - d-форма (а = 0,30750 нм при 1143°С, z = 2, пространств. группа Im3m, плотн. 6,28 г/см3); DH0 полиморфных переходов (в кДж/моль) a : b 2,2, b : d 2,1, d : g 1,9. При охлаждении до комнатной т-ры g-форма переходит в тетрагон. кристаллич. модификацию (а = 0,3774 нм, с = 0,3525 нм, плотн. 7,21 г/см3). Т. пл. 1244°С, т. кип. ок. 2080 °С; С°р [в Дж/(моль.К)] a-формы 26,3, b 26,5, g 27,6; DH0пл 12,0 кДж/моль, DH0исп 227 кДж/моль; ур-ния температурной зависимости давления пара lgр (Пa)= 10,8828 — 13625/Т (1043 [ Т [ 1158 К) и lgp (Па) = 20,005 - 14850/T - 2,52 lgT(1517 [ T [ 2353 К); температурный коэф. линейного расширения (в К-1) в интервале 0-20oС для a-Мn 2,23 • 10-5, b 2,49 • 10-5, g 1,475 • 10-5; r (в мкОм.см) для a-Mn ~ 140, b 91, g 35-40; температурный коэф. r (в К-1) для a-Мn (2-3).10-4, b 1,36.10-3, g (5,5-6,5).10-3; теплопроводность 66,5 Вт/(см.К). Ниже — 173°С М. антифeрромагнитен, при более высоких т-рах парамагнитен; магн. восприимчивость +9,6.10-6. Модификации a, b и d хрупкие, g-Mn пластичен, но после деформации медленно разрушается; твердость по шкале Роквелла a-Мn 70, g-Мn 20. М. легко окисляется на воздухе, образуя выше 800°С окалину, состоящую из внутр. слоя МnО и внеш. слоя Мn3О4. Ниже 800 °С образуется Мn2О3, а при т-рах ниже 450°С - МnО2 (см. Марганца оксиды). Поглощает Н2 (до 60 см3 на 100 г М.) с образованием твердых р-ров. М. взаимод. с галогенами, давая дигалогениды МnХ2 (с фтором также MnF3 и MnF4) - кристаллы; хорошо раств. в воде (кроме MnF2); образуют кристаллогидраты (см. также табл.). Для MnBr2 т. пл. 698 °С, MnI2 638°С. Дихлорид MnCl2 получают взаимод. MnО2 с конц. соляной к-той или Mn, MnО либо MnСО3 с газообразным НCl; применяют для получения пигментов, как катализатор в орг. синтезе, реагент для обнаружения S2O82- , IO4-, для обработки семян с целью ускорения роста растений, в физ.-хим. анализе как репер.
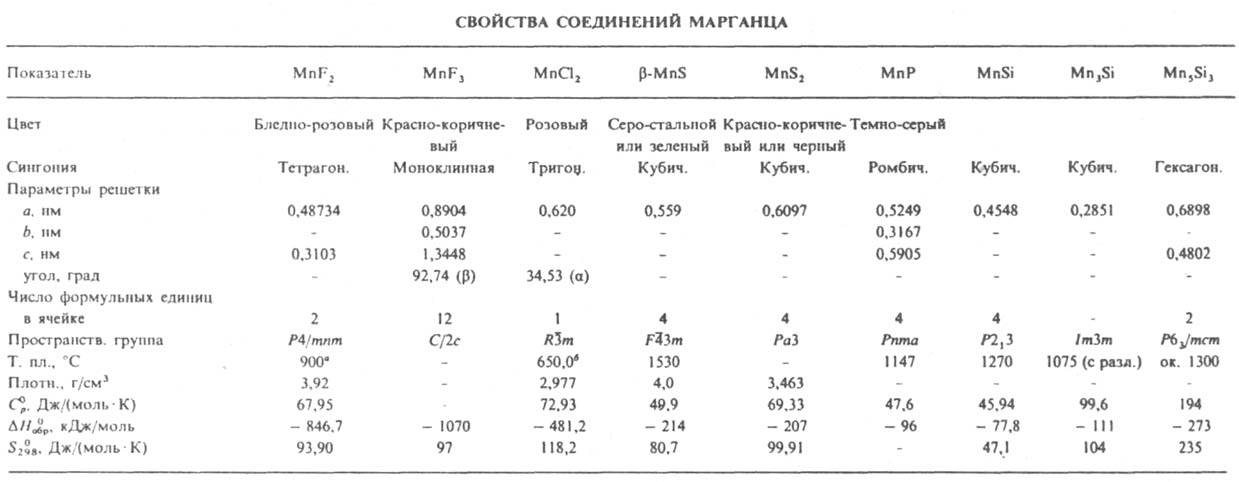
* Т. кип. ок. 1640°С; DH0пл 14 кДж/моль, DH0исп 256 кДж/моль. * Т. кип. 1240°С; DH0пл 37,6 кДж/моль, DH0исп 148 кДж/моль.
Трихлорид MnCl3 образуется при взаимод. MnО2 с р-ром НCl в этаноле при - 63 °С; при нагр. до 40 °С разлагается с выделением Cl2. Быстрым охлаждением паров, образующихся при взаимод. MnF3 с F2 при т-рах выше 550°С, получают тетрафторид MnF4 - голубые кристаллы; при нагр. до 70 °С разлагается с выделением F2; DH0обр -1109 кДж/молъ.
При нагр. М. взаимод. с S, N2, P, С, Si и др. неметаллами. Известны нитриды: MnN6, Mn5N2, Mn4N, MnN, Mn6N5, Mn3N2 и MnxN с х = 9,2-25,3. Сульфид MnS существует в трех кристаллич. модификациях (b-форма - минерал алабандин); плохо раств. в воде и м. б. осажден из р-ров солей Mn2+ сульфидами щелочных металлов.
Фосфиды М.: MnР, MnР3, Mn2Р (т. пл. 1327°С), Mn3Р (т. пл. 1105°C), Mn3P2 (разлагается при 1090 °С) и Mn4Р (т. пл. 1085°С с разл.).
Карбиды М.: Mn3С [разлагается при 950°С, С°р 93,3 Дж/(моль.К), DH0обр 5,6 кДж/моль, S0298 98,7 Дж/(моль.К)], Mn5С2 (разлагается при 1050 °С, DH0обр -66,1 кДж/моль), Mn15С4 (разлагается при 850 °С), Mn7С3 [разлагается при 1100°С, DH0обр -98,7 кДж/моль, S0298 217 Дж/(моль.К)], Mn23С6 (разлагается при 1025 °С, DH0обр -287 кДж/моль), Mn2С7. Макс. р-римость углерода в a-, b- и g-Mn соотв. равна 1,3, 0,4 и 2,0% по массе.
Силициды М.: MnSi, MnSi1,7 [т. пл. 1160°С с разл., C0p 58,70 Дж/(моль.К), DH0обр -83,7 кДж/моль, S0298 55,5 Дж/(моль.К)], Mn3Si, Mn5Si3.
М. взаимод. с водой при комнатной т-ре очень медленно, при нагр. - с умеренной скоростью. Реагирует с разб. соляной и азотной к-тами и с горячей H2SO4 с образованием солей Mn2+ . Из р-ров солей Mn2+ (см. Марганца карбонат. Марганца нитрат. Марганца сульфат) при рН 8,7 осаждается плохо растворимый в воде Mn(ОН)2 - слабое основание. Еще более слабые основные св-ва проявляет нерастворимый в воде гидроксид Mn(III). Известны неустойчивые соли ортомарганцоватистой Н4MnО4 и марганцоватистой Н3MnО4 к-т. наиб. важны соли марганцоватой к-ты Н2MnО4 - манганаты и марганцовой к-ты НMnО4 - перманганаты (см. Манганаты).
Получение. М. получают методами металлотермии - карбо-, силико- или алюминотермич. восстановлением рудных концентратов, а также выщелачиванием руд H2SO4 с послед. электролитич. восстановлением MnSO4. Предварительно руды М. обогащают, иногда обжигают (для разложения карбонатов), восстанавливают (для перевода в соед. Mn2+) или сплавляют с кварцитом.
Карботермич. восстановлением получают высокоуглеродистый ферромарганец (содержащий 6-8% С), силикотермическим - низкоуглеродистый ферромарганец ( ~ 0,1% С), алюминотермическим - чистый М. Металлич. М. с низким содержанием С и Fe получают также восстановлением концентратов силикомарганцем (содержит более 36% Si).
Hаиб. чистый М. с концентрацией примесей металлов менее 0,1% получают электролизом р-ров MnSO4 (с концентрацией 35-40 г/л) в присут. (NH4)2SO4 (ок. 150 г/л) при рН 8,0-8,5. Для очистки от газовых примесей жидкий М. вакуумируют или перегоняют в вакууме.
Определение. Качественно Mn3+ обнаруживают по красно-фиолетовому окрашиванию, возникающему при добавлении р-ров солей Mn3+ к щелочному р-ру формальдоксима, или по коричневому пятну, появляющемуся на фильтровальной бумаге (смоченной предварительно р-ром 8-гидроксихинолина) после нанесения капли р-ра соли Mn3+ .
Количественно М. определяют спектрофотометрически в виде иона MnО4 (предварительно Mn2+ и Mn3+ окисляют до MnО4 избытком КIO4 в среде HNO3-H3PO4).
Из р-ров Mn2+ м.б. осажден в виде MnS действием (NH4)2S; осадок имеет сначала светло-розовый цвет, к-рый при нагр. переходит в зеленый.
Применение. М. один из основных металлов, используемых
для раскисления, десульфурации и легирования сталей (более 90% производимого М. применяют в металлургии). Для удаления из стали О и S М. вводят в виде высокоуглеродистого ферромарганца (8-9 кг на 1 т стали), для легирования стали-в виде средне- и малоуглеродистого ферромарганца. М. - компонент сплавов цветных металлов, сплавов с Аl и Mg. М. придает стали, Аl и Mg прочность, твердость, улучшает способность к закаливанию, устойчивость к коррозии. М. применяют также для получения сплавов на его основе и для создания защитных антикоррозионных покрытий на металлах.
В капиталистич. странах в произ-ве соед. М. ежегодно используется ок. 800 тыс. т марганцевых руд (о применении соед. М. см. соответствующие статьи), в произ-ве марганцевоцинковых ферритов, применяемых для изготовления трансформаторов и др. радиотехн. устройств, для получения окрашенного стекла и цветных глазурей, для фосфатирования стальных изделий - ок. 10 тыс. т/год.
Произ-во марганцевого концентрата (тыс. т, в пересчете на металл): в Австралии 1750, Бразилии 2000, Габоне 2200, Гане 290, Индии 1400, ЮАР 3200 (1985); в СССР 9876 (1983).
М. необходим для жизнедеятельности организмов. Недостаток М. у растений вызывает хлороз (недостаток хлорофилла). Нек-рые почвы бедны М. и нуждаются в марганцевых удобрениях. Недостаток М. в организме человека (суточная доза составляет ок. 4 мг) также может вызывать заболевания. В то же время соед. М. токсичны, поражают центр. нервную систему, вдыхание пыли из соед. М. в течение 1-3 лет может привести к хронич. отравлениям; ПДК (в пересчете на М.) для М. как аэрозоля конденсации 0,03 мг/м , как аэрозоля дезинтеграции 0,2 мг/м3, при одновременном воздействии М. и фтора 0,15 мг/м3.
М. открыл К. Шееле и выделил в чистом виде Ю. Ган в 1774.
Лит.: Позин М. Е., Технология минеральных солей, 4 изд., ч. 1, Л., 1974; Электрохимия марганца, т. 1-8, Тб., 1957-1979; Kemmitt R. D. W., Peacock R. D., The chemistry of manganese, technetium and rhenium, Oxf, 1975 (Pergamon texts in inorganic chemistry, v. 22). Э. Г. Раков.

