Словарь научных терминов
Ион-радикалы
ИОН-РАДИКАЛЫ, частицы с нсспаренным электроном и зарядом. По знаку заряда различают катион-радикалы (КР) и анион-радикалы (АР). И.-р. могут быть органическими и неорганическими.
Органические И.-р. Практически любая орг. молекула может образовывать как АР (при восстановлении), так и КР (при окислении). Относит. склонность к образованию КР или АР зависит от природы атомов, входящих в молекулу, и от особенностей ее строения. Напр., ароматич. тиоэфиры ArSCH3 дают стабильные КР ArSCH3+' и АР ArSCH3-'. Ароматич. амины преим. образуют КР ArNR2+', а ароматич. кетоны - АР Аr2СО-' (т. наз. кетилы). Устойчивость И.-р. возрастает с увеличением степени делокализации неспаренного электрона. Наличие в молекуле электронодонорных групп (OR, NR2, CR=CR2 и др.) повышает стабильность КР, акцепторных (NO2, CN, COOR, SO2R, CF3 и др.) - АР. Нек-рые соли И. р. выделены в твердом виде (см., напр., Металлы органические). В газовой фазе И. р. образуются при электронном ударе, диссоциативной ионизации (см. Маcс-спектрометрия), а также в условиях ион-циклотронного резонанса. Для жидкой фазы общий метод - электрохим. окисление или восстановление. АР получают также р-цией субстратов с сольватированным электроном или донорами электронов, в качестве к-рых используют щелочные и щел.-зем. металлы, др. орг. АР, орг. анионы и нек-рые соед. с низким потенциалом ионизации. В качестве окислителей при получении КР используют H2SO4, к-ты Льюиса (АlСl3, SbCl5 и др.), РbО2, K3[Fe(CN)6], NO+ClO4-, орг. катионы, орг. соед. с высоким сродством к электрону (хиноны, тетрацианоэтилен и др.), стабильные радикалы, напр., ароксильные, нитроксильные, гидразильные. Иногда КР получают восстановлением, напр.:
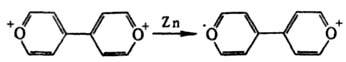
Образованию И.-р. при взаимод. донора и акцептора электронов предшествует перенос заряда в донорно-акцепторном комплексе, чему способствует УФ облучение. И.-р. - интермедиаты мн. р-ций; образуются из субстратов в результате одноэлектронного переноса. Для И.-р. характерны р-ции фрагментации, напр.:
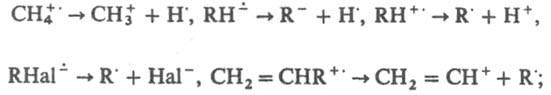
диспропорционирования (р-ция 1) и димеризации (р-ция 2):
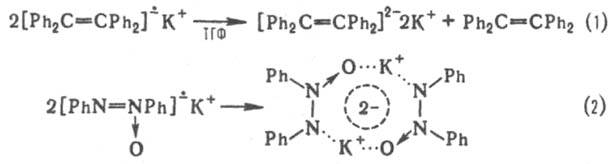
Р-ции (1) и (2) обусловлены рекомбинацией радикальных частиц, однако необходимое для этого сближение двух И.-р. затрудняется их зарядовым расталкиванием. Последнее уменьшается, если И.-р. входит в состав ионной пары. И.-р. способны вступать в гетеролитич. р-ции, в результате к-рых могут образовываться новые связи или происходить одноэлектронный перенос с регенерацией нейтральной орг. молекулы, напр.:
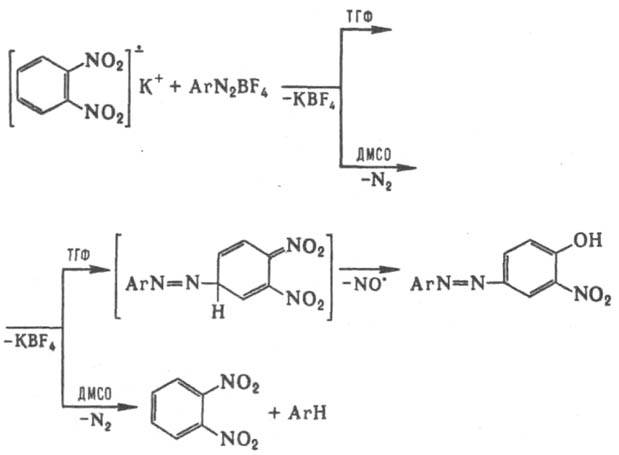
Неорганические И.-р. Наиб. известен АР кислорода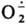 , т. наз. супероксид-ион, входящий в состав КО2 (см. Калий) и образующийся при его диссоциации в непротоногенном р-рителе, напр., бензоле, в присут. 18-краун-6-эфира. Образуется
, т. наз. супероксид-ион, входящий в состав КО2 (см. Калий) и образующийся при его диссоциации в непротоногенном р-рителе, напр., бензоле, в присут. 18-краун-6-эфира. Образуется 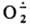 также при электролизе О2 и при одноэлектронном переносе типа:
также при электролизе О2 и при одноэлектронном переносе типа:
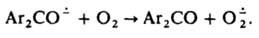
Супероксид устойчив в отсутствие протонов; является умеренно сильным восстановителем и очень слабым окислителем. Его окислит. способность возрастает в присут. сильных протонных к-т. Сильный нуклеофил, реагирует, напр., с ароматич. дисульфидами: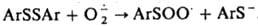 Супероксид выступает как переносчик электрона в процессах дыхания, идущих С участием супероксиддисмутазы. Возможно, что в тканях под действием
Супероксид выступает как переносчик электрона в процессах дыхания, идущих С участием супероксиддисмутазы. Возможно, что в тканях под действием 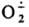 нек-рые прир. антибиотики дают АР, далее превращающиеся в более активные противомикробные и канцеролитич. соед. Так, напр., объясняют образование реумицина из ксантотрицина.
нек-рые прир. антибиотики дают АР, далее превращающиеся в более активные противомикробные и канцеролитич. соед. Так, напр., объясняют образование реумицина из ксантотрицина.
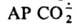 получают электрохим. восстановлением СО2 при потенциале —2 В или из формиат-иона по схеме:
получают электрохим. восстановлением СО2 при потенциале —2 В или из формиат-иона по схеме:
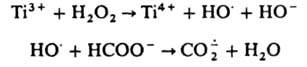
Потенциал восстановления м. б. значительно снижен при использовании в качестве катализатора комплекса Ni с 1,4,8,11-тетраазациклотетрадеканом. Возможно, что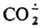 образуется при фотосинтезе.
образуется при фотосинтезе. 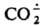 - восстановитель, напр.:
- восстановитель, напр.:
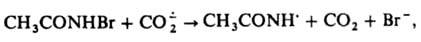
способен присоединяться по кратным связям:
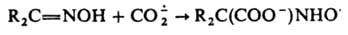
Перспективное св-во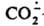 - его способность превращаться в СО, что позволяет получать последний из СО2.
- его способность превращаться в СО, что позволяет получать последний из СО2.
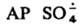 образуется при фотолизе и термолизе р-ров персульфатов или при добавлении к ним солей переходных металлов в низких степенях окисления, напр.:
образуется при фотолизе и термолизе р-ров персульфатов или при добавлении к ним солей переходных металлов в низких степенях окисления, напр.:
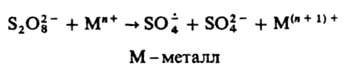
Наиб. эффективна смесь солей Fe2+ и Сu+. С орг. соед.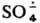 обычно дает КР, напр.,
обычно дает КР, напр., 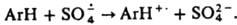 Атом Н при этом обычно не отщепляется.
Лит.: Морковник А. С., Охлобыстин О. Ю., "Успехи химии", 1979, т. 48, в. 11, с. 1968-2006; их же, "Химия гстероцикл. соединений", 1980, № 8, с. 1011-29; Росси Р. А., де Росси Р. X., Ароматическое замещение по механизму SRN 1, пер. с англ., М., 1986; Тодрес З. В., Ион-радикалы в органическом синтезе, М., 1986; Julliard М., Chanon М., "Chem. Rev." 1983, v. 83, № 4, p. 425-506. 3. В. Тодрес.
Атом Н при этом обычно не отщепляется.
Лит.: Морковник А. С., Охлобыстин О. Ю., "Успехи химии", 1979, т. 48, в. 11, с. 1968-2006; их же, "Химия гстероцикл. соединений", 1980, № 8, с. 1011-29; Росси Р. А., де Росси Р. X., Ароматическое замещение по механизму SRN 1, пер. с англ., М., 1986; Тодрес З. В., Ион-радикалы в органическом синтезе, М., 1986; Julliard М., Chanon М., "Chem. Rev." 1983, v. 83, № 4, p. 425-506. 3. В. Тодрес.
Органические И.-р. Практически любая орг. молекула может образовывать как АР (при восстановлении), так и КР (при окислении). Относит. склонность к образованию КР или АР зависит от природы атомов, входящих в молекулу, и от особенностей ее строения. Напр., ароматич. тиоэфиры ArSCH3 дают стабильные КР ArSCH3+' и АР ArSCH3-'. Ароматич. амины преим. образуют КР ArNR2+', а ароматич. кетоны - АР Аr2СО-' (т. наз. кетилы). Устойчивость И.-р. возрастает с увеличением степени делокализации неспаренного электрона. Наличие в молекуле электронодонорных групп (OR, NR2, CR=CR2 и др.) повышает стабильность КР, акцепторных (NO2, CN, COOR, SO2R, CF3 и др.) - АР. Нек-рые соли И. р. выделены в твердом виде (см., напр., Металлы органические). В газовой фазе И. р. образуются при электронном ударе, диссоциативной ионизации (см. Маcс-спектрометрия), а также в условиях ион-циклотронного резонанса. Для жидкой фазы общий метод - электрохим. окисление или восстановление. АР получают также р-цией субстратов с сольватированным электроном или донорами электронов, в качестве к-рых используют щелочные и щел.-зем. металлы, др. орг. АР, орг. анионы и нек-рые соед. с низким потенциалом ионизации. В качестве окислителей при получении КР используют H2SO4, к-ты Льюиса (АlСl3, SbCl5 и др.), РbО2, K3[Fe(CN)6], NO+ClO4-, орг. катионы, орг. соед. с высоким сродством к электрону (хиноны, тетрацианоэтилен и др.), стабильные радикалы, напр., ароксильные, нитроксильные, гидразильные. Иногда КР получают восстановлением, напр.:
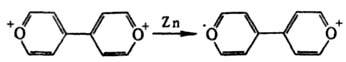
Образованию И.-р. при взаимод. донора и акцептора электронов предшествует перенос заряда в донорно-акцепторном комплексе, чему способствует УФ облучение. И.-р. - интермедиаты мн. р-ций; образуются из субстратов в результате одноэлектронного переноса. Для И.-р. характерны р-ции фрагментации, напр.:
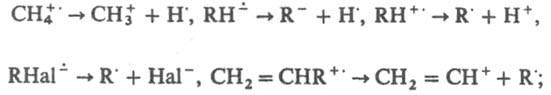
диспропорционирования (р-ция 1) и димеризации (р-ция 2):

Р-ции (1) и (2) обусловлены рекомбинацией радикальных частиц, однако необходимое для этого сближение двух И.-р. затрудняется их зарядовым расталкиванием. Последнее уменьшается, если И.-р. входит в состав ионной пары. И.-р. способны вступать в гетеролитич. р-ции, в результате к-рых могут образовываться новые связи или происходить одноэлектронный перенос с регенерацией нейтральной орг. молекулы, напр.:

Неорганические И.-р. Наиб. известен АР кислорода
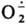 , т. наз. супероксид-ион, входящий в состав КО2 (см. Калий) и образующийся при его диссоциации в непротоногенном р-рителе, напр., бензоле, в присут. 18-краун-6-эфира. Образуется
, т. наз. супероксид-ион, входящий в состав КО2 (см. Калий) и образующийся при его диссоциации в непротоногенном р-рителе, напр., бензоле, в присут. 18-краун-6-эфира. Образуется 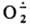 также при электролизе О2 и при одноэлектронном переносе типа:
также при электролизе О2 и при одноэлектронном переносе типа:
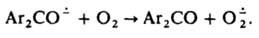
Супероксид устойчив в отсутствие протонов; является умеренно сильным восстановителем и очень слабым окислителем. Его окислит. способность возрастает в присут. сильных протонных к-т. Сильный нуклеофил, реагирует, напр., с ароматич. дисульфидами:
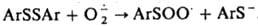 Супероксид выступает как переносчик электрона в процессах дыхания, идущих С участием супероксиддисмутазы. Возможно, что в тканях под действием
Супероксид выступает как переносчик электрона в процессах дыхания, идущих С участием супероксиддисмутазы. Возможно, что в тканях под действием 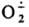 нек-рые прир. антибиотики дают АР, далее превращающиеся в более активные противомикробные и канцеролитич. соед. Так, напр., объясняют образование реумицина из ксантотрицина.
нек-рые прир. антибиотики дают АР, далее превращающиеся в более активные противомикробные и канцеролитич. соед. Так, напр., объясняют образование реумицина из ксантотрицина.
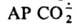 получают электрохим. восстановлением СО2 при потенциале —2 В или из формиат-иона по схеме:
получают электрохим. восстановлением СО2 при потенциале —2 В или из формиат-иона по схеме:
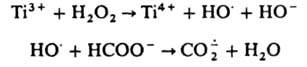
Потенциал восстановления м. б. значительно снижен при использовании в качестве катализатора комплекса Ni с 1,4,8,11-тетраазациклотетрадеканом. Возможно, что
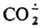 образуется при фотосинтезе.
образуется при фотосинтезе. 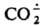 - восстановитель, напр.:
- восстановитель, напр.:
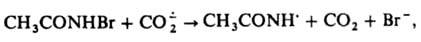
способен присоединяться по кратным связям:
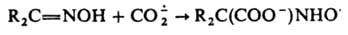
Перспективное св-во
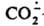 - его способность превращаться в СО, что позволяет получать последний из СО2.
- его способность превращаться в СО, что позволяет получать последний из СО2.
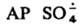 образуется при фотолизе и термолизе р-ров персульфатов или при добавлении к ним солей переходных металлов в низких степенях окисления, напр.:
образуется при фотолизе и термолизе р-ров персульфатов или при добавлении к ним солей переходных металлов в низких степенях окисления, напр.:
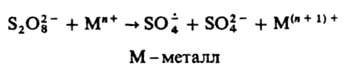
Наиб. эффективна смесь солей Fe2+ и Сu+. С орг. соед.
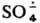 обычно дает КР, напр.,
обычно дает КР, напр., 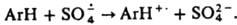 Атом Н при этом обычно не отщепляется.
Лит.: Морковник А. С., Охлобыстин О. Ю., "Успехи химии", 1979, т. 48, в. 11, с. 1968-2006; их же, "Химия гстероцикл. соединений", 1980, № 8, с. 1011-29; Росси Р. А., де Росси Р. X., Ароматическое замещение по механизму SRN 1, пер. с англ., М., 1986; Тодрес З. В., Ион-радикалы в органическом синтезе, М., 1986; Julliard М., Chanon М., "Chem. Rev." 1983, v. 83, № 4, p. 425-506. 3. В. Тодрес.
Атом Н при этом обычно не отщепляется.
Лит.: Морковник А. С., Охлобыстин О. Ю., "Успехи химии", 1979, т. 48, в. 11, с. 1968-2006; их же, "Химия гстероцикл. соединений", 1980, № 8, с. 1011-29; Росси Р. А., де Росси Р. X., Ароматическое замещение по механизму SRN 1, пер. с англ., М., 1986; Тодрес З. В., Ион-радикалы в органическом синтезе, М., 1986; Julliard М., Chanon М., "Chem. Rev." 1983, v. 83, № 4, p. 425-506. 3. В. Тодрес.
Иванова реакция
Игданит
Идеальный газ
Идентификация
Изатин
Изафенин
Избирательность анализа
Известковые удобрения
Известняк
Известь
Измельчение
Изо..
Изоmeризat
Изоамилацетат
Изоамиловый спирт
Изобутилен
Изобутиловый спирт
Изовалериановая кислота
Изовалериановый альдегид
Изоиндол
Изоксазол
Изолейцин
Изолированная система
Изолобальной аналогии принцип
Изоляционные масла
Изомасляный альдегид
Изомеразы
Изомеризация
Изомерия
Изомерия атомных ядер
Изоморфизм
Изоникотиновая кислота
Изонитрилы
Изонитрильные комплексы переходных металлов
Изопрен
Изопреновые каучуки синтетические
Изопреноиды
Изопропаноламины
Изопропилбензол
Изопропиловый спирт
Изотактические полимеры
Изотахофорез
Изотиазол
Изотиоцианаты
Изотопного разбавления метод
Изотопные генераторы
Изотопные индикаторы
Изотопные эффекты
Изотопный анализ
Изотопный обмен
Изотопов разделение
Изотопы
Изоферменты
Изофталевая кислота
Изофталоилхлорид
Изохинолин
Изохинолиновые алкалоиды
Изоцианаты
Изоцианаты блокированные
Изоцинхомероновая кислота
Изоцитрат-лиаза
Изоэвгенол
Изоэлектрическая точка
Изумрудная зелень
Илиды
Имид-амидная перегруппировка
Имидазол
Имидазолины
Имидофосфаты
Имиды карболовых кислот
Имиды металлов
Имизин
Иминиевые соли
Иминоксильные радикалы
Иминоэфиры
Иммерсионные жидкости
Иммобилизованные ферменты
Иммуномодулирующие средства
Иммунохимия
Импедансный метод
Импульсный радиолиз
Импульсный фотолиз
Ингибиторы
Ингибиторы коррозии
Индазол
Индамины
Индан
Индандионы
Индантрон
Инден
Индиго
Индигоидные красители
Индигокармин
Индий
Индикаторная бумага
Индикаторные трубки
Индикаторы
Индия антимонид
Индия арсенид
Индия галогениды
Индия оксиды
Индия фосфид
Индоанилины
Индоксан
Индол
Индольные алкалоиды
Индофенолы
Индуктивный эффект
Индукция химическая
Индулины
Индустриальные масла
Инженерная энзимология
Инициаторы радикальные
Инициирование
Инициирующие взрывчатые вещества
Инкапаситанты
Инозин
Инозиты
Инсектициды
Инсулин
Интенсивные параметры
Интеркалаты
Интерлейкины
Интермедиат
Интерметаллиды
Интерфероны
Инулин
Инфразвуковые аппараты
Инфракрасная спектроскопия
Иод
Иодбензол
Иодиды
Иодное число
Иодные удобрения
Иодозобензол
Иодометрия
Ион-молекулярные комплексы
Ион-радикалы
Ион-циклотронный резонанс
Ионизации потенциал
Ионизирующие излучения
Иониты
Ионная атмосфера
Ионная имплантация
Ионная полимеризация
Ионная хроматография
Ионно-молекулярные реакции
Ионного рассеяния спектроскопия
Ионные кристаллы
Ионные пары
Ионные радиусы
Ионный выход
Ионный микроанализ
Ионный обмен
Ионол
Иономеры
Ионометрия
Иононы
Ионообменная хроматография
Ионообменные смолы
Ионоселективные электроды
Ионофоры
Ионы
Ионы в газах
Иоцича реакция
Иприт
Ипсо-замещение
Иридий
Иридийорганические соединения
Ирисаль
Ирританты
Искусственная пища
Искусственные волокна
Искусственный интеллект
Испарение
Итаконовая кислота
Иттербий
Иттрий
Ихтиоциды
Июпак

